
CANERGY® 100 mg Comprimés pour chiens
DECHRA Veterinary Products SASComprimé
Composition
Principes actifs et excipients
Principes actifs
| Nom du principe actif | Quantité de principe actif |
|---|---|
| Propentofylline | 100 mg |
Clinique
Indications d'utilisation par espèce
- Chien
Amélioration de la circulation vasculaire périphérique et cérébrale.
Amélioration des états d’apathie, de léthargie et du comportement général.
Voie d'administration et posologie
Voie d'administration
- Orale
Posologie
"
La posologie recommandée est de 6,0 à 10,0 mg de propentofylline par kg de poids corporel par jour, à répartir sur deux doses, comme suit:
Poids corporel (kg) Matin Soir Nombre total de comprimés par jour Dose quotidienne totale (mg/kg) 5 - 8 1/4 1/4 1/2 6,25 - 10,0 > 8 - 10 1/2 1/4 3/4 7,5 - 9,4 > 10 - 15 1/2 1/2 1 6,7 - 10,0 > 15 - 25 3/4 3/4 1 1/2 6,0 - 10,0 > 25 - 33 1 1 2 6,1 - 8,0 > 33 - 49 1 1/2 1 1/2 3 6,1 - 9,1 > 49 - 66 2 2 4 6,1 - 8,2 > 66 - 83 2 1/2 2 1/2 5 6,0 - 7,6 Les comprimés peuvent être administrés directement dans la gueule du chien, à l'arrière de la langue, ou mélangés à une petite boule de nourriture, et ils doivent être administrés au moins 30 minutes avant le repas.
Les comprimés peuvent être divisés en 2 ou 4 fractions égales pour obtenir l'exacte posologie nécessaire. Placez le comprimé sur une surface plate, avec la barre de sécabilité tournée vers le haut et la face convexe (arrondie) tournée vers le plan de travail.
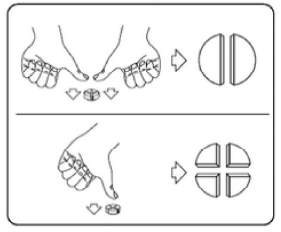
Moitiés: appuyez avec vos pouces des deux côtés du comprimé
Quarts: appuyez avec votre pouce au centre du comprimé.
Temps d'attente
Complément d'information temps d'attente
Sans objet.
Contre indications
Ne pas utiliser chez les chiens pesant moins de 5 kg.
Ne pas utiliser en cas d’hypersensibilité connue à la substance active ou à l’un des excipients.
Voir aussi la rubrique « Utilisation en cas de gestation, de lactation ou de ponte ».
Mises en garde particulières à chaque espèce cible
Aucune.
Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Ne pas utiliser chez les chiens pesant moins de 5 kg.
Ne pas utiliser en cas d’hypersensibilité connue à la substance active ou à l’un des excipients.
Voir aussi la rubrique « Utilisation en cas de gestation, de lactation ou de ponte ».
Précautions particulières à prendre par la personne qui administre le médicament
Des précautions doivent être prises afin d’éviter toute ingestion accidentelle.
En cas d’ingestion accidentelle des comprimés, demander immédiatement conseil à un médecin et lui montrer la notice ou l’étiquetage.
Se laver les mains après utilisation.
Les morceaux de comprimés inutilisés doivent être réinsérés dans les espaces libres de la plaquette, et remis dans la boîte en carton et être utilisés lors de l’administration suivante.
Précautions particulières concernant la protection de l'environnement
Aucune.
Autres précautions
Aucune.
Interactions médicamenteuses et autres formes d'interaction
Aucune connue.
Utilisation en cas de gravidité de lactation ou de ponte
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et/ou de lactation. L’utilisation du produit n’est donc pas recommandée chez les chiennes gestantes ou allaitantes ni chez les animaux destinés à la reproduction.
Effets indésirables
Dans de rares cas (entre 1 et 10 animaux sur 10 000), des réactions cutanées allergiques, des vomissements et des troubles cardiaques ont été signalés. Dans un tel cas, le traitement doit être interrompu.
Surdosage (symptômes, conduite d’urgences, antidotes)
Excitation, tachycardie, hypotension, rougissement des muqueuses et vomissements.
À l’arrêt du traitement, ces symptômes se résorbent spontanément.
Informations pharmacologiques ou immunologiques
codes ATC
QC04AD90 : propentofylline
Pharmacodynamie
Groupe pharmacothérapeutique : vasodilatateur périphérique ; dérivés de la purine ; propentofylline.
Il a été montré que la propentofylline améliore le débit sanguin, en particulier dans le cœur et le muscle squelettique. Elle augmente également le débit sanguin dans le cerveau et donc son approvisionnement en oxygène, sans pour autant augmenter les besoins du cerveau en glucose. Elle exerce un effet chronotrope positif d’ampleur modérée et un effet ionotrope positif marqué. Par ailleurs, il a été montré qu’elle exerce un effet anti-arythmique chez les chiens atteints d’ischémie myocardique et une action bronchodilatatrice équivalente à celle de l’aminofylline.
La propentofylline inhibe l’agrégation plaquettaire et améliore les propriétés rhéologiques des érythrocytes.
Elle exerce un effet direct sur le cœur et réduit la résistance vasculaire périphérique, atténuant ainsi l’effort cardiaque.
La propentofylline peut amener l’animal à faire plus volontiers de l’exercice et améliorer sa tolérance à l’effort, en particulier chez les chiens âgés.
Pharmacocinétique et environnement
Après administration orale, la propentofylline est rapidement et totalement absorbée et fait l’objet d’une rapide distribution dans les tissus. Les concentrations plasmatiques maximales sont atteintes en 15 minutes après administration orale chez le chien.
La demi-vie est d’environ 30 minutes et la biodisponibilité de la substance mère est d’environ 30 %. Il existe un certain nombre de métabolites actifs et la biotransformation se déroule principalement dans le foie. La propentofylline est excrétée à hauteur de 80 – 90 % sous la forme de métabolites par l’intermédiaire des reins. Le reste est éliminé dans les selles. Aucune bioaccumulation n’est constatée.
Données pharmaceutiques
Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans
Durée de conservation des fractions de comprimé après première ouverture du conditionnement primaire : 4 jours.
Température de conservation
Pas de précautions particulières de conservation concernant la température.
Toute fraction de comprimé inutilisée doit être réintroduite dans la plaquette ouverte et replacée dans la boîte dans l’attente de l’administration suivante.
Précautions particulières de conservation selon pertinence
Des précautions doivent être prises afin d’éviter toute ingestion accidentelle.
En cas d’ingestion accidentelle des comprimés, demander immédiatement conseil à un médecin et lui montrer la notice ou l’étiquetage.
Se laver les mains après utilisation.
Les morceaux de comprimés inutilisés doivent être réinsérés dans les espaces libres de la plaquette, et remis dans la boîte en carton et être utilisés lors de l’administration suivante.
Précautions particulières à prendre lors de l'élimination de médicaments non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régis par la réglementation sur les déchets.
Nature et composition du conditionnement primaire
Titulaire de l'autorisation de mise sur le marché
LE VET. BEHEER
WILGENWEG 7 3421 TV OUDEWATER PAYS-BAS
Présentations commercialisées et AMM
| Présentation | GTIN | Numéro d'autorisation de mise sur le marché | Date de première mise sur le marché (ou AMM) | Classement du médicament en matière de délivrance | Accessible aux groupements |
|---|---|---|---|---|---|
| CANERGY® 100 mg Boîte de 10 plaquettes thermoformées de 10 comprimés quadrisécables | 05701170450255 | FR/V/7121327 - 9/2015<br /><br />Date de mise à jour du texte : 17/06/2020 | 4/28/2015 | Soumis à prescription | Oui |
Responsable de la mise sur le marché
DECHRA Veterinary Products SAS
60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX
Responsable de la Pharmacovigilance
DECHRA Veterinary Products SAS
60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX
