
Composition
Principes actifs et excipients
Principes actifs
| Nom du principe actif | Quantité de principe actif |
|---|---|
| Métronidazole | 100 mg/comprimé |
Excipients
| Nom de l'excipient |
|---|
| Cellulose microcristalline |
| Carboxyméthylamidon sodique type A |
| Hydroxypropylcellulose |
| Levure déshydratée |
| Arôme de bœuf |
| Stéarate de magnésium |
Clinique
Indications d'utilisation par espèce
- Chien
- Chat
- Traitement des infections gastro-intestinales dues à Giardia spp. et Clostridia spp. (i.e. C. perfringens ou C. difficile).
- Traitement des infections de l'appareil urogénital, de la cavité buccale, de la gorge et de la peau dues aux bactéries anaérobies strictes (par ex. Clostridia spp.) sensibles au métronidazole.
Voie d'administration et posologie
Voie d'administration
- Orale
Posologie
- Chien
- Chat
La dose recommandée de métronidazole est de 50 mg par kg de poids corporel par jour, pendant 5 à 7 jours. La dose quotidienne peut être répartie en deux prises quotidiennes (à savoir 25 mg/kg de poids corporel deux fois par jour).
Pour garantir l’administration d'une dose correcte, le poids corporel doit être déterminé aussi précisément que possible. Le tableau ci-dessous sert de guide pour l’administration du produit à la dose recommandée de 50 mg par kg de poids corporel, administrée une fois par jour ou, de préférence, deux fois par jour à raison de 25 mg par kg de poids corporel.
Nombre de comprimés
Deux fois par jour
Une fois par jour
Poids corporel (kg)
Matin
Soir
0,5 kg
¼
-
¼
1 kg
¼
¼
½
2 kg
½
½
1
3 kg
¾
¾
1 ½
4 kg
1
1
2
5 kg
1 ¼
1 ¼
2 ½
6 kg
1 ½
1 ½
3
7 kg
1 ¾
1 ¾
3 ½
8 kg
2
2
4
 = ¼ comprimé
= ¼ comprimé  = ½ comprimé
= ½ comprimé  = ¾ comprimé
= ¾ comprimé  = 1 comprimé
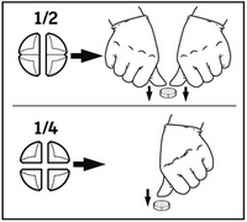
= 1 compriméLes comprimés peuvent être divisés en 2 ou 4 parties égales pour assurer un dosage précis. Placez le comprimé sur une surface plane, le côté rainuré vers le haut et le côté convexe (arrondi) vers la surface.
Moitiés : appuyez avec vos pouces des deux côtés du comprimé.
Quarts : appuyez avec votre pouce au centre du comprimé.
Temps d'attente
Complément d'information temps d'attente
Sans objet.
Contre indications
Ne pas utiliser en cas de troubles hépatiques.
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Mises en garde particulières à chaque espèce cible
Aucune.
Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
En raison de la probable variabilité (temporelle, géographique) de la survenue de bactéries résistantes au métronidazole, un échantillonnage bactériologique et un test de sensibilité sont recommandés.
Dans la mesure du possible, le produit ne doit être utilisé que sur la base d’un test de sensibilité.
Les réglementations officielles, nationales et régionales en matière d'utilisation des agents antimicrobiens doivent être prises en compte lors de l’utilisation du médicament vétérinaire.
Dans de très rares cas, des signes neurologiques peuvent survenir, en particulier après un traitement prolongé avec le métronidazole.
Précautions particulières à prendre par la personne qui administre le médicament
Le métronidazole présente des propriétés mutagènes et génotoxiques avérées chez les animaux de laboratoire ainsi que chez l’être humain. Le métronidazole est un cancérogène avéré chez les animaux de laboratoire et a des effets cancérogènes possibles chez l'être humain. Cependant, il n’y a pas assez de preuves chez l'être humain pour confirmer la cancérogénicité du métronidazole.
Le métronidazole peut être nocif pour le fœtus.
Des gants imperméables doivent être portés lors de l’administration du produit afin d’éviter tout contact cutané.
Pour éviter toute ingestion accidentelle, en particulier par un enfant, les comprimés et les parties de comprimés non utilisés doivent être remis dans la plaquette ouverte, qui doit être replacée dans l’emballage externe et conservée dans un endroit sûr, hors de la vue et de la portée des enfants. En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette. Se laver soigneusement les mains après avoir manipulé les comprimés.
Le métronidazole peut provoquer des réactions d’hypersensibilité. En cas l’hypersensibilité connue au métronidazole, évitez tout contact avec le médicament vétérinaire.
Précautions particulières concernant la protection de l'environnement
Sans objet.
Autres précautions
Aucune.
Interactions médicamenteuses et autres formes d'interaction
Le métronidazole peut avoir un effet inhibiteur sur la dégradation d’autres médicaments dans le foie, tels que la phénytoïne, la ciclosporine et la warfarine.
La cimétidine peut réduire le métabolisme hépatique du métronidazole, ce qui peut entraîner une augmentation de la concentration sérique du métronidazole.
Le phénobarbital peut augmenter le métabolisme hépatique du métronidazole, ce qui peut entraîner une réduction de la concentration sérique du métronidazole.
Utilisation en cas de gravidité de lactation ou de ponte
Gestation :
Les études réalisées sur des animaux de laboratoire ont montré des résultats contradictoires en ce qui concerne les effets tératogènes/embryotoxiques du métronidazole. En conséquence, l'utilisation du produit n'est pas recommandée pendant la gestation.
Lactation :
Le métronidazole est excrété dans le lait et son utilisation pendant la lactation n’est donc pas recommandée.
Effets indésirables
Les effets indésirables suivants peuvent survenir après l’administration du métronidazole : vomissements, hépatotoxicité, neutropénie et signes neurologiques.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
Surdosage (symptômes, conduite d’urgences, antidotes)
Des effets indésirables sont plus susceptibles de se produire à des doses et des durées de traitement dépassant le schéma thérapeutique recommandé. Si des signes neurologiques apparaissent, le traitement doit être interrompu et le patient doit être traité de manière symptomatique.
Informations pharmacologiques ou immunologiques
codes ATC
QP51AA01 : métronidazole
Pharmacodynamie
Après pénétration du métronidazole à l’intérieur des bactéries, la molécule est réduite par les bactéries sensibles (anaérobies). Les métabolites créés ont un effet toxique sur les bactéries en se liant à l’ADN bactérien. De manière générale, le métronidazole a une activité bactéricide sur les bactéries sensibles à des concentrations égales ou légèrement supérieures à la concentration minimale inhibitrice (CMI).
Pharmacocinétique et environnement
Le métronidazole est immédiatement et bien absorbé après l’administration orale. La biodisponibilité du métronidazole est de pratiquement 100 %.
Chez les chiens, une Cmax de 79,5 µg/mL est observée 1 heure après l’administration orale d’une dose unique de 62 mg/kg de poids corporel. La demi-vie plasmatique terminale est d’environ 5,3 heures (3,5 à 7,3 heures).
Chez les chats, une Cmax de 93,6 µg/mL est observée 1,5 heure après l’administration orale d’une dose unique de 83 mg/kg de poids corporel. La demi-vie plasmatique terminale est d’environ 6,7 heures (5,2 à 8,3 heures).
Le métronidazole pénètre bien dans les tissus et les fluides corporels, tels que la salive, le lait, les sécrétions vaginales et le sperme. Le métronidazole est principalement métabolisé dans le foie. Dans les 24 heures qui suivent l’administration orale, 35 à 65 % de la dose administrée (métronidazole et ses métabolites) sont excrétés dans l’urine.
Données pharmaceutiques
Incompatibilités majeures
Aucune connue.
Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 3 ans.
Durée de conservation après ouverture
Durée de conservation des comprimés divisés : 3 jours.
Précautions particulières de conservation selon pertinence
Ce médicament vétérinaire ne nécessite aucune condition de stockage particulière.
Précautions particulières à prendre lors de l'élimination de médicaments non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Nature et composition du conditionnement primaire
Plaquette thermoformée aluminium - PVC/PE/PVDC
Titulaire de l'autorisation de mise sur le marché
LIVISTO INT’L
AV. UNIVERSITAT AUTONOMA, 29
08290 CERDANYOLA DEL VALLES (BARCELONA)
Espagne
Présentations commercialisées et AMM
| Présentation | GTIN | Numéro d'autorisation de mise sur le marché | Date de première mise sur le marché (ou AMM) | Classement du médicament en matière de délivrance | Accessible aux groupements |
|---|---|---|---|---|---|
| Boîte de 10 plaquettes thermoformées de 10 comprimés quadrisécables | 08436565583764 | FR/V/7713509 8/2019 | Soumis à prescription | Non |
Responsable de la mise sur le marché
Responsable de la Pharmacovigilance
Compléments d'informations
Date de mise à jour du RCP
3/8/2023Gamme thérapeutique
Gamme thérapeutique
AntibiotiquePathogènes (genre)
- Clostridium
- Giardia
