TEVEMYXINE 3 400 UI/ML + 10 000 UI/ML POUDRE ET SOLVANT POUR COLLYRE EN SOLUTION POUR CHIENS ET CHATS
Identification
- Dénomination du médicament vétérinaire
- TEVEMYXINE 3 400 UI/ML + 10 000 UI/ML POUDRE ET SOLVANT POUR COLLYRE EN SOLUTION POUR CHIENS ET CHATS
- Forme pharmaceutique
- Poudre et solvant pour collyre en solution
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Néomycine (sous forme de sulfate) 3400 UI/mL Polymyxine B (sous forme de sulfate) 10000 UI/mL - Excipients
Nom de l'excipient Quantité de l'excipient Chlorure de benzalkonium 0.1 mg/mL Dextran 70 pour préparations injectables Dihydrogénophosphate de sodium dihydraté Phosphate disodique dodécahydraté Chlorure de sodium Eau pour préparations injectables Édétate disodique - Informations supplémentaires
Lyophilisat : Lyophilisat blanc à crème.
Solvant : Solution pratiquement limpide, incolore et pratiquement sans particules.
Solution reconstituée : Solution pratiquement limpide, incolore à jaune pâle, pratiquement sans particules.
Lyophilisat Un flacon contient : Substances actives : Néomycine....................................................................
(sous forme de sulfate)
17 000 UI
Polymyxine B ...............................................................
(sous forme de sulfate)
50 000 UI
Excipients : Édétate disodique
Dextran 70 pour préparations injectables
Eau pour préparations injectables
Solvant Un flacon de 5 mL contient : Excipients : Chlorure de benzalkonium.......................................... 0,50 mg
Dextran 70 pour préparations injectables
Dihydrogénophosphate de sodium dihydraté
Phosphate disodique dodécahydraté (E339(ii))
Chlorure de sodium
Eau pour préparations injectables
Solution reconstituée Un mL contient : Substances actives : Néomycine....................................................................
(sous forme de sulfate)
3 400 UI
Polymyxine B ...............................................................
(sous forme de sulfate)
10 000 UI
Excipients : Chlorure de benzalkonium......................................... 0,10 mg
Dextran 70 pour préparations injectables
Dihydrogénophosphate de sodium dihydraté
Phosphate disodique dodécahydraté
Chlorure de sodium
Eau pour préparations injectables
Édétate disodique
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Traitement des infections oculaires à germes sensibles à la polymyxine et à la néomycine. |
- Contre-indications
Ne pas utiliser en cas d’hypersensibilité aux substances actives ou à l’un des excipients.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Aucune.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Aucune.
- Précaution particulière à prendre par la personne qui administre le médicament
Se laver les mains après manipulation.
Les personnes présentant une hypersensibilité connue à l'un des composants doivent éviter tout contact avec le médicament vétérinaire.
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
Sans objet.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Gestation et lactation :
L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
- Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
Effets indésirables et surdosage
- Incompatibilité majeure
Aucune connue.
- Effets indésirables
Chez les chiens et les chats :
Très rare
(
Irritation oculaire, douleur oculaire1. 1Ces signes ont été observés lors de l'instillation du collyre.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| En moyenne, instiller 2 gouttes de collyre 3 à 4 fois par jour. Durée moyenne du traitement : 8 à 10 jours.
Mode d'emploi
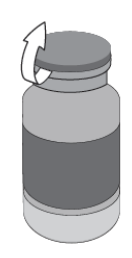
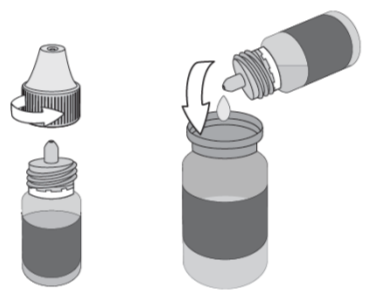
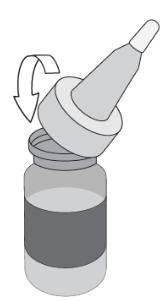
Se laver soigneusement les mains avant de manipuler et de reconstituer la solution de collyre afin d’éviter toute contamination microbiologique du médicament vétérinaire. Il est recommandé de faire réaliser la reconstitution du collyre par un vétérinaire ou un pharmacien.
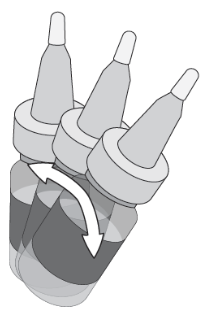
Retirer le capuchon du compte-gouttes pour administrer le médicament vétérinaire. Maintenir la tête du chien/chat dans une position légèrement verticale. Tenir le récipient en position verticale sans toucher l’œil. Poser la main/le petit doigt sur le front du chien/chat pour maintenir une distance entre le récipient et l’œil. Tirer la paupière de l’œil affecté vers le bas, ce qui formera une petite poche dans la paupière. Presser délicatement le compte-gouttes pour administrer deux gouttes dans la poche créée en tirant la paupière. Veiller à ne pas toucher l’embout du compte-gouttes après avoir ouvert le récipient et remettre le capuchon en place après utilisation. |
Temps d'attente
- Voie d'administration
- Oculaire
Conservation et stockage
- Température de conservation
- Non renseigné
- Précautions particulières de conservation selon pertinence
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| TEVEMYXINE® Collyre Boîte de 1 flacon de lyophilisat, 1 flacon de solvant de 5 mL et 1 compte-gouttes | Non | Soumis à prescription | FR/V/7976637 9/1992 |
Informations de révision
- Date de révision de la notice
- 7/11/2025
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- DÔMES PHARMA
- Z.A.C. de Champ Lamet 3 rue André Citroën 63430 PONT-DU-CHÂTEAU
http://www.domespharma.com
- Responsable de la mise sur le marché
- DÔMES PHARMA FR - Gamme vétérinaire
- DÔMES PHARMA FR - Division Vétérinaire -57 rue des Bardines 63370 LEMPDES
https://www.domespharma.fr/
- Responsable de la pharmacovigilance
- DÔMES PHARMA FR - Gamme vétérinaire
- DÔMES PHARMA FR - Division Vétérinaire -57 rue des Bardines 63370 LEMPDES
+33 (0)4 63 66 33 90
https://www.domespharma.fr/