PREVICOXⓇ 227 mg comprimés à croquer pour chiens
Identification
- Dénomination du médicament vétérinaire
- PREVICOXⓇ 227 mg comprimés à croquer pour chiens
- Forme pharmaceutique
- Comprimé à croquer
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Firocoxib 227 mg - Excipients
Nom de l'excipient Lactose monohydraté Cellulose microcristalline Arôme fumée Hydroxypropylcellulose Croscarmellose sodique Stéarate de magnésium Caramel (E 150d) Silice colloïdale anhydre Oxyde de fer jaune (E 172) Oxyde de fer rouge (E 172) - Informations supplémentaires
Chaque comprimé à croquer contient :
Substance active :
Firocoxib …………………………………………………………………… 227 mg
Apparence :
Comprimés à croquer brun clair ronds convexes avec une barre de cassure cruciforme sur une face. Les comprimés à croquer peuvent être divisés en 2 ou 4 fractions égales.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Soulagement de la douleur et de l’inflammation associées à l’arthrose chez le chien. Soulagement de la douleur post-opératoire et de l’inflammation associée à la chirurgie des tissus mous, à la chirurgie orthopédique et à la chirurgie dentaire chez le chien. |
- Contre-indications
Ne pas utiliser chez les chiennes gestantes ou en lactation.
Ne pas utiliser chez les animaux âgés de moins de 10 semaines ou pesant moins de 3 kg.
Ne pas utiliser chez des animaux présentant un saignement gastro-intestinal, un trouble de la coagulation sanguine ou des troubles hémorragiques.
Ne pas utiliser en association avec des corticostéroïdes ou d’autres anti-inflammatoires non stéroïdiens (AINS).
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Aucune.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Ne pas dépasser la dose recommandée, voir rubrique « Posologie et voie d'administration ».
L’utilisation chez de très jeunes animaux, ou chez des animaux atteints d’insuffisance rénale, cardiaque ou hépatique (suspectée ou confirmée), peut entraîner des risques supplémentaires. Si une telle utilisation ne peut être évitée, celle-ci devra être effectuée sous surveillance vétérinaire stricte.
Éviter d’utiliser chez des animaux déshydratés, en hypovolémie ou en hypotension, en raison du risque accru de toxicité rénale. Toute association avec des produits ayant un potentiel néphrotoxique doit être évitée.
En cas de risque de saignement gastro-intestinal ou en cas d’intolérance connue aux AINS, le produit doit être utilisé sous surveillance vétérinaire stricte. Des troubles rénaux et/ou hépatiques ont été rapportés dans de très rares occasions chez des chiens ayant reçu le traitement à la dose recommandée. Il est possible qu’une proportion de tels cas soit due à une pathologie hépatique ou rénale subclinique antérieure au début du traitement. Par conséquent, des examens de laboratoire appropriés pour établir les paramètres biochimiques rénaux ou hépatiques de base sont recommandés avant et périodiquement pendant l'administration.
Le traitement doit être interrompu en présence d’un des signes suivants : diarrhées à répétition, vomissements, sang occulte dans les selles, perte de poids soudaine, anorexie, léthargie, dégradation des paramètres biochimiques hépatiques ou rénaux.
- Précaution particulière à prendre par la personne qui administre le médicament
Se laver les mains après utilisation du produit.
En cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Remettre les fractions de comprimés dans l’emballage d’origine.
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
Sans objet.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation et lactation :
Ne pas utiliser chez les chiennes gestantes ou en lactation.
Les études de laboratoire sur les lapins ont mis en évidence des effets maternotoxiques et fœtotoxiques, à des doses proches de celles recommandées pour le chien.
- Interactions médicamenteuses et autres formes d'interactions
Un traitement préalable par d’autres anti-inflammatoires peut entraîner l’apparition ou l’aggravation d’effets indésirables. Il est donc recommandé d’observer une période de 24 heures sans traitement avant de commencer le traitement avec le médicament vétérinaire. La durée de cette période de transition doit cependant être adaptée en fonction des propriétés pharmacocinétiques des produits utilisés précédemment.
Ne pas administrer le médicament vétérinaire simultanément avec d’autres AINS ou des glucocorticoïdes. Des ulcères gastro-intestinaux peuvent être exacerbés par les corticostéroïdes chez les animaux recevant des anti-inflammatoires non-stéroïdiens.
Un traitement simultané avec des molécules ayant un effet sur le flux sanguin rénal, telles que les diurétiques ou les inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA), doit faire l’objet d’un suivi clinique. Toute association avec des produits ayant un potentiel néphrotoxique doit être évitée en raison d’un risque accru de toxicité rénale. Les produits anesthésiques pouvant affecter la perfusion rénale, une fluidothérapie parentérale doit être envisagée pendant l’opération afin de réduire de potentielles complications rénales lors de l’utilisation d’AINS en péri-opératoire.
L’utilisation simultanée d’autres principes actifs fortement liés aux protéines peut entraîner une compétition avec le firocoxib sur les sites de liaison, et avoir par conséquent des effets toxiques.
- Anti-microbiens et anti-parasitaires : lutte contre les résistances
Sans objet.
Effets indésirables et surdosage
- Incompatibilité majeure
Sans objet.
- Effets indésirables
Chiens :
Peu fréquent
(1 à 10 animaux / 1 000 animaux traités) :
Vomissements1 et diarrhées1 Rare
(1 à 10 animaux / 10 000 animaux traités) :
Symptômes nerveux Très rare
(< 1 animal / 10 000 animaux traités, y compris les cas isolés) :
Troubles hépatiques et troubles rénaux (1) : Généralement passagères et réversibles à l'arrêt du traitement.
Si des effets secondaires apparaissent tels que vomissements, diarrhées à répétition, sang occulte dans les selles, perte de poids soudaine, anorexie, léthargie, dégradation des paramètres biochimiques hépatiques ou rénaux, le traitement doit être interrompu et un vétérinaire doit être consulté. Comme lors de l’utilisation d’autre AINS, des effets secondaires très graves peuvent avoir lieu et, dans des cas très rares, peuvent engager le pronostic vital.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Voie orale.
Arthrose : Administrer 5 mg/kg de poids vif en une fois par jour selon le tableau ci-dessous. Les comprimés peuvent être mélangés ou non à l’alimentation. La durée du traitement varie selon la réponse observée. Comme la durée des études de terrain était limitée à 90 jours, la mise en place d’un traitement plus long devrait être évaluée avec attention et faire l’objet d’un suivi vétérinaire régulier.
Soulagement de la douleur post-opératoire : Administrer une dose quotidienne de 5 mg/kg de poids vif selon le tableau ci-dessous, jusqu’à 3 jours si nécessaire. La première dose est administrée environ 2 heures avant l’opération.
Après une chirurgie orthopédique et en fonction de la réponse observée, le traitement peut être poursuivi après les 3 premiers jours, en suivant la même posologie quotidienne et laissé à l’appréciation du vétérinaire traitant.
Les comprimés peuvent être divisés en 2 à 4 fractions égales pour permettre un ajustement précis de la dose.
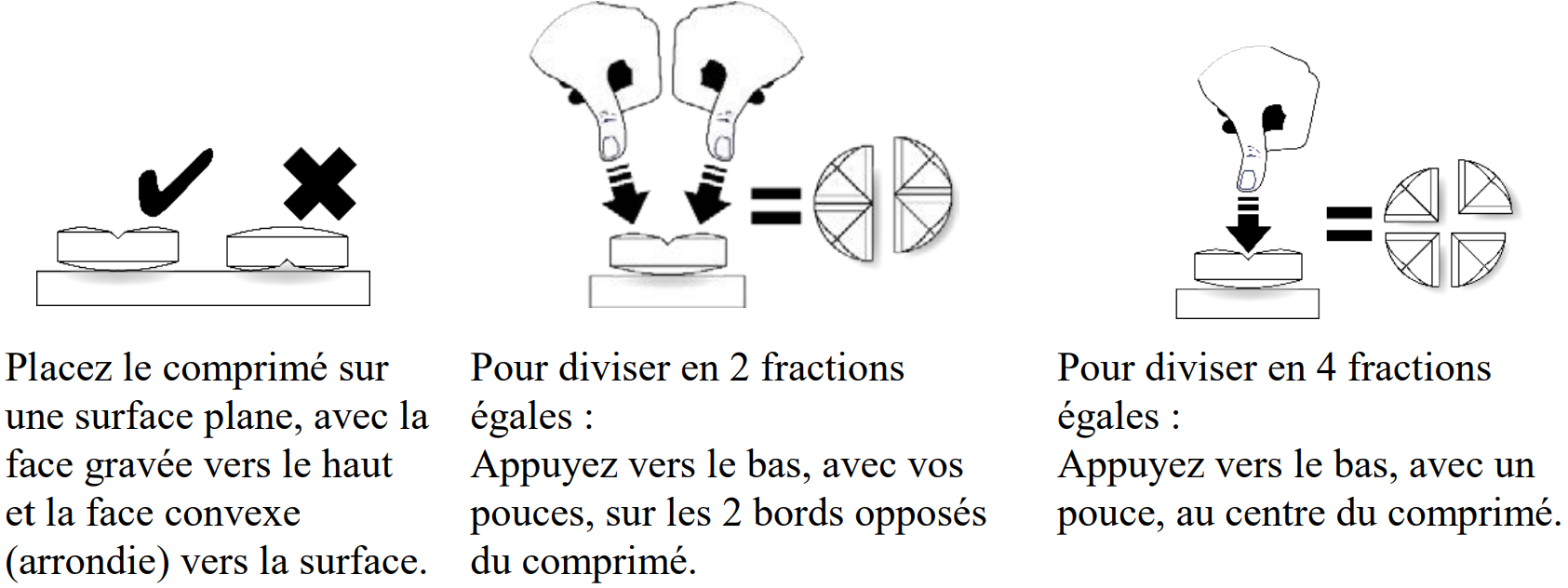
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Temps d'attente
- Voie d'administration
- Orale
Conservation et stockage
- Température de conservation
À conserver à une température ne dépassant pas 30 °C.
- Précautions particulières de conservation selon pertinence
À conserver dans l'emballage d'origine.
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| PREVICOXⓇ227 mg comprimés à croquer pour chiens Boîte en carton contenant 3 plaquettes de 10 comprimés (30 comprimés) | Non | Soumis à prescription | EU/2/04/045/004 |
| PREVICOXⓇ 227 mg comprimés à croquer pour chiens Boîte en carton contenant 1 flacon de 60 comprimés | Non | Soumis à prescription | EU/2/04/045/009 |
| PREVICOXⓇ 227 mg comprimés à croquer pour chiens Boîte en carton contenant 18 plaquettes de 10 comprimés (180 comprimés) | Non | Soumis à prescription | EU/2/04/045/006 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- Boehringer Ingelheim Vetmedica GmbH
- BINGER STRASSE 173
55216 INGELHEIM AM RHEIN
ALLEMAGNE
- Responsable de la mise sur le marché
- BOEHRINGER INGELHEIM ANIMAL HEALTH FRANCE SCS
- 29 avenue Tony Garnier
69007 LYON
FRANCEhttps://www.boehringer-ingelheim.fr/
- Responsable de la pharmacovigilance
- BOEHRINGER INGELHEIM ANIMAL HEALTH FRANCE SCS
- 29 avenue Tony Garnier
69007 LYON
FRANCE04 72 72 30 00
https://www.boehringer-ingelheim.fr/
