FLUBENOL Pâte
Identification
- Dénomination du médicament vétérinaire
- FLUBENOL Pâte
- Forme pharmaceutique
- Pâte orale
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Flubendazole 44 mg/mL - Excipients
Nom de l'excipient Quantité de l'excipient Parahydroxybenzoate de méthyle (E 218) 1.8 mg/mL Parahydroxybenzoate de propyle (E 216) 0.2 mg/mL Glycérol Carbomères Hydroxyde de sodium Eau purifiée - Informations supplémentaires
Pâte orale inodore, de couleur blanche à crème.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Affections à parasites sensibles au flubendazole : Traitement des helminthoses digestives dues à : |
- Contre-indications
Aucune connue.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Aucune.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Aucune.
- Précaution particulière à prendre par la personne qui administre le médicament
Se laver les mains après usage.
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
-
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
L’innocuité du médicament vétérinaire chez les femelles en gestation ou allaitantes a été établie.
Gestation et lactation :
Peut être utilisé au cours de la gestation et de la lactation.
Les études de laboratoire sur les rats et les lapins n’ont pas mis en évidence d’effets tératogènes ou embryotoxiques du flubendazole à la dose utilisée en thérapeutique.
- Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
Effets indésirables et surdosage
- Incompatibilité majeure
Aucune connue.
- Effets indésirables
Chiens et chats.
Très rare
(<1 animal / 10 000 animaux traités, y compris les cas isolés):
Diarrhée1, vomissements2 1 Modérée
2 Transitoires
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie |
|---|---|
| 22 mg de flubendazole par kg de poids corporel et par jour, soit 1 mL de pâte par 2 kg de poids corporel par jour.
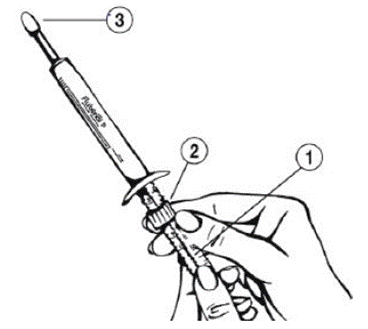
Mode d’administration : Tenir l’applicateur d'une main au niveau du piston et avec l'autre main ajuster la bague de dosage en la tournant en fonction du poids corporel de l'animal de sorte que le bord supérieur de la bague (2) corresponde au repère du poids (kg) de l’animal (1). Retirez le capuchon (3) et appuyez sur le piston de l'applicateur jusqu'à ce qu'il s'arrête. Pour chaque traitement ultérieur, ajoutez le poids corporel de l'animal et ajustez le dosage ; par exemple pour un chat de 5 kg devant être traité pendant 3 jours consécutifs, le bord supérieur de la bague de dosage (2) est réglé à 5 kg pour le premier jour de traitement, 10 kg pour le deuxième jour de traitement et 15 kg pour le troisième jour de traitement.
La dose recommandée est introduite directement dans la gueule du chien ou du chat ou bien mélangée à la nourriture (cette méthode est recommandée avec les animaux agressifs ou difficiles à immobiliser). |
Temps d'attente
- Voie d'administration
- Orale
Conservation et stockage
- Température de conservation
À conserver à une température ne dépassant pas 25°C.
- Précautions particulières de conservation selon pertinence
- Non renseigné
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| Boîte de 1 applicateur gradué de 7,5 mL de pâte | Non | Non soumis à prescription | FR/V/1709197 6/1991 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- ELANCO
- Heinz-Lohmann-Strasse 4
27472 Cuxhaven
Allemagne
- Responsable de la mise sur le marché
- ELANCO FRANCE
- Crisco Uno, Bâtiment C
3-5 avenue de la Cristallerie
92310 Sèvres - Francehttp://www.elanco.fr
- Responsable de la pharmacovigilance
- ELANCO FRANCE
- Crisco Uno, Bâtiment C
3-5 avenue de la Cristallerie
92310 Sèvres - France+33 1 55 49 35 29
http://www.elanco.fr