DuOticⓇ 10mg/1mg Gel auriculaire pour chiens
Identification
- Dénomination du médicament vétérinaire
- DuOticⓇ 10mg/1mg Gel auriculaire pour chiens
- Forme pharmaceutique
- Gel auriculaire
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Terbinafine 10 mg Acétate de Bétaméthasone 1 mg - Excipients
Nom de l'excipient Quantité de l'excipient Butylhydroxytoluène (E321) 1 mg Acide oléique Lécithine Hypromellose Carbonate de propylène Glycérol Phormal - Informations supplémentaires
Gel translucide blanc cassé à légèrement jaune.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Traitement de l'otite externe associée à Malassezia pachydermatis. |
- Contre-indications
Ne pas utiliser en cas d’hypersensibilité aux substances actives, à d’autres corticoïdes ou à l’un des excipients.
Ne pas utiliser en cas de perforation du tympan.
Ne pas utiliser chez les chiens présentant une démodécie généralisée.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Nettoyer les oreilles avant d’appliquer le premier traitement. Dans les essais cliniques, seule une solution saline a été utilisée pour nettoyer les oreilles avant la première application du médicament vétérinaire ; ensuite, les oreilles n’ont plus été nettoyées pendant toute la durée de l’étude (45 jours).
Si le traitement par ce médicament vétérinaire est interrompu, les conduits auditifs doivent être nettoyés avant d’instaurer un traitement par un autre produit. Une humidité transitoire du pavillon interne et externe peut être observée après administration.
Cette observation est attribuée à la présence du médicament vétérinaire et ne pose pas de problème clinique. L’otite fongique est souvent secondaire à d'autres affections.
Il convient d'établir un diagnostic approprié et de rechercher une thérapie pour les affections causales avant d’envisager un traitement antimicrobien.
Chez les animaux ayant des antécédents d’otites externes chroniques ou récurrentes, l’efficacité du médicament vétérinaire peut être réduite si des causes sous-jacentes de l’affection, telles qu’une allergie ou la conformation anatomique de l’oreille, ne sont pas traitées.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
L’innocuité du médicament vétérinaire n'a pas été établie chez les chiens âgés de moins de 2 mois ou pesant moins de 1,4 kg. L’utilisation du médicament vétérinaire doit être basée sur l’identification et les tests de sensibilité des agents pathogènes cibles. Si cela s’avère possible, le traitement doit reposer sur des informations épidémiologiques et sur la connaissance de la sensibilité des agents pathogènes cibles ou au niveau local/régional. L'utilisation du médicament vétérinaire doit être conforme aux politiques antimicrobiennes officielles, nationales et régionales. Toute utilisation du médicament vétérinaire produit ne respectant pas les instructions formulées dans le RCP peut accroître la prévalence de champignons résistants à la terbinafine et peut réduire l’efficacité du traitement par d'autres agents antifongiques. En cas d'otite externe parasitaire ou bactérienne, un traitement acaricide ou antibiotique doit être mis en œuvre, selon les besoins. Avant l’application du médicament vétérinaire, le conduit auditif externe doit être examiné avec soin afin de s'assurer que le tympan n'est pas perforé (voir rubrique 3.3). L’utilisation prolongée et intensive de préparations corticoïdes topiques est connue pour induire des effets systémiques, incluant une suppression de la fonction surrénale (voir rubrique 3.10). Une diminution des taux de cortisol a été observée après instillation du produit dans des études de tolérance utilisant un produit apparenté (avant et après stimulation par l’ACTH) ; cette observation indique que la bétaméthasone est absorbée et pénètre dans la circulation systémique. Cette observation n’était pas corrélée à des signes pathologiques ou cliniques et s’est avérée réversible. L'utilisation concomitante de corticoïdes doit être évitée. Utiliser avec prudence chez les chiens présentant une affection endocrinienne suspectée ou confirmée (c'est-à-dire un diabète sucré, une hypo- ou hyperthyroïdie, etc.). Le médicament vétérinaire peut provoquer une irritation des yeux. Éviter tout contact accidentel avec les yeux du chien. En cas d'exposition oculaire accidentelle, rincer les yeux abondamment à l'eau pendant 10 à 15 minutes. Si des signes cliniques apparaissent, consulter un vétérinaire.Dans de très rares cas, des problèmes oculaires tels qu’une kératoconjonctivite sèche et des ulcères cornéens ont été rapportés chez des chiens traités par un produit apparenté, en l’absence de tout contact oculaire avec le produit. Bien qu’aucun lien de causalité n’ait pu être établi avec certitude avec le médicament vétérinaire, il est important de recommander aux propriétaires la surveillance de tout signe oculaire (tel que strabisme, rougeur et écoulement) dans les heures et les jours qui suivent l’application du produit, et de consulter rapidement un vétérinaire si de tels signes apparaissent. L’innocuité et l’efficacité du médicament vétérinaire chez le chat n'ont pas été évaluées. Les données de pharmacovigilance montrent que l’utilisation du produit chez le chat peut être associée à des signes neurologiques (y compris le syndrome de Horner avec protrusion des membranes nictitantes, myosis, anisocorie, et troubles de l'oreille interne avec ataxie et inclinaison de la tête) et systémiques (anorexie et léthargie). L'utilisation du médicament vétérinaire chez le chat doit donc être évitée.
- Précaution particulière à prendre par la personne qui administre le médicament
Le médicament vétérinaire peut provoquer une irritation des yeux. Une exposition oculaire accidentelle peut survenir lorsque le chien secoue la tête durant ou immédiatement après l’administration. Pour éviter ce risque pour les propriétaires, il est recommandé que ce médicament vétérinaire ne soit administré que par les vétérinaires ou sous leur stricte surveillance. Il y a lieu d'adopter des mesures adéquates (p. ex. port de lunettes de sécurité durant l’administration, bien masser le conduit auditif après l’administration pour permettre une distribution homogène du médicament vétérinaire, limiter les mouvements du chien après l’administration) afin d’éviter toute exposition dans les yeux. Éviter tout contact entre les mains et les yeux. En cas d'exposition oculaire accidentelle, rincer abondamment les yeux à l'eau pendant 10 à 15 minutes. Si des symptômes apparaissent, consulter un médecin et lui montrer la notice ou l'étiquette. En cas de contact accidentel avec la peau, laver abondamment la peau exposée avec de l’eau. En cas d'ingestion accidentelle chez l’être humain, consulter immédiatement un médecin et lui montrer la notice ou l'étiquette.
- Précautions particulières concernant la protection de l'environnement
Sans objet
- Autres précautions
Sans objet
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation et lactation : La bétaméthasone est tératogène chez les animaux de laboratoire. L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Ne pas utiliser durant la gestation et la lactation.
Fertilité : Ne pas utiliser sur les animaux destinés à la reproduction
- Interactions médicamenteuses et autres formes d'interactions
La compatibilité avec les nettoyants auriculaires autres que la solution saline n’a pas été démontrée.
- Anti-microbiens et anti-parasitaires : lutte contre les résistances
Sans objet
Effets indésirables et surdosage
- Incompatibilité majeure
Sans objet
- Effets indésirables
Peu fréquent (1 à 10 animaux / 1 000 animaux traités) : Élévation des enzymes hépatiquesa Très rare (<1 animal / 10 000 animaux traités, y compris les cas isolés) : Surdité, troubles de l’auditionc Réactions au niveau de la zone d’application (érythème, douleur, prurit, œdème, ulcère) Réactions d’hypersensibilité (y compris œdème facial, urticaire, choc)c aÉlévation principalement transitoire de l'alanine aminotransférase bGénéralement temporaire. Principalement chez les animaux âgés
cEn cas d'hypersensibilité à l’un des composants, laver soigneusement l’oreille
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir également la rubrique « Coordonnées » de la notice.
Posologie
| Espèce(s) | Posologie |
|---|---|
| Administrer un tube par oreille affectée. Répéter l’administration après 7 jours. La réponse clinique maximale peut n'être observée que 21 jours après la deuxième administration (28 jours après le début du traitement).
Il est recommandé de nettoyer et de sécher le conduit auditif externe avant la première administration du médicament vétérinaire.
1. Ouvrir le tube par un mouvement de torsion sur l'embout souple.
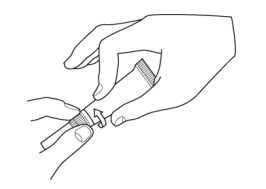
2. Introduire cet embout souple flexible dans le conduit auditif.
3. Appliquer le produit dans le canal auditif en comprimant le tube entre deux doigts.
Après application, la base de l'oreille peut être massée brièvement et délicatement pour favoriser la répartition uniforme du médicament vétérinaire dans le conduit auditif. |
Temps d'attente
- Voie d'administration
- Auriculaire
Conservation et stockage
- Température de conservation
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
- Précautions particulières de conservation selon pertinence
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| DuOtic 10mg/1mg Ger auriculaire pour chiens, 20 tubes | Oui | Soumis à prescription | EU/2/24/327/001-003 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la pharmacovigilance
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX01.30.48.71.40
https://www.dechra.fr/
