EQUILIS® Strep E
Identification
- Dénomination du médicament vétérinaire
- EQUILIS® Strep E
- Forme pharmaceutique
- Lyophilisat et solvant pour suspension injectable
Composition
- Principes actifs
Nom du principe actif Streptococcus equi - Excipients
Nom de l'excipient Stabilisateur NAO-1 Eau pour injections - Informations supplémentaires
Par dose de 0,2 ml de vaccin :
Substance active :
Streptococcus equi, souche vivante TW928, mutante délétée ……….. 109,0 à 109,4 ufc1
1 unités formant colonieExcipients :
Stabilisateur NAO-1
Eau pour injections.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Immunisation active des chevaux contre Streptococcus equi, afin de réduire les signes cliniques et la formation d’abcès au niveau des noeuds lymphatiques.
|
- Contre-indications
Aucune.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Une diffusion de la souche vaccinale à partir du site d'injection peut être observée pendant une durée de 4 jours après la vaccination.
Dans la littérature scientifique, il est décrit qu'un très faible nombre de chevaux peuvent être atteints de purpura hémorragique lorsqu'ils sont vaccinés peu de temps après une infection. Aucun cas de purpura hémorragique n'a été observé au cours d'aucune des études d'innocuité réalisées pendant le développement d'EQUILIS® Strep E. L'incidence du purpura hémorragique étant très faible, sa survenue ne peut pour autant être complétement exclue.
Au cours des études expérimentales d'efficacité réalisées par le laboratoire, une protection insuffisante a été observée chez environ 1/4 des chevaux vaccinés avec la dose recommandée.
Ne pas administrer d'antibiotiques durant la semaine qui suit la vaccination.
La souche vaccinale est sensible aux pénicillines, aux tétracyclines, aux macrolides et à la lincomycine.
La souche vaccinale est résistante aux aminoglycosides, aux sulfalmides, à la fluméquine et aux associations triméthoprime-sulfa.- Précautions particulières pour une utilisation sûre chez les espèces cibles
Seuls les chevaux en bonne santé doivent être vaccinés.
S’assurer que le lyophilisat est entièrement reconstitué avant utilisation.
La primovaccination réalisée pendant un épisode infectieux n’est pas efficace, car l’immunité est insuffisante tant que la primovaccination n’a pas été achevée.- Précaution particulière à prendre par la personne qui administre le médicament
Pour l’utilisateur :
Ce produit contient une souche vaccinale vivante mutante délétée ayant une capacité de croissance limitée dans les tissus de mammifères. L’auto-injection accidentelle peut provoquer une réaction inflammatoire entraînant une forte douleur et un gonflement. Des précautions particulières devront être prises lors de la fixation de l’embout sur la seringue pour prévenir tout risque de blessure avec l’aiguille. En cas d’auto-injection accidentelle, même en quantité minime, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquetage.
Pour le médecin :
Ce produit contient une souche vaccinale vivante mutante délétée auxotrophe, Streptococcus equi, ayant une virulence atténuée. Cependant, les composants bactériens de ce produit peuvent provoquer une réaction inflammatoire, accompagnée d’un oedème important et douloureux, lors d’une injection accidentelle.
Un traitement antiinflammatoire est conseillé même si seulement une quantité minime de produit est injectée. Un traitement antibiotique additionnel devra être envisagé pour des raisons de sécurité. La sensibilité de cette souche vaccinale aux antibiotiques est listée ci-dessus (voir rubrique mises en gardes particulières).
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Ne pas utiliser chez les juments gestantes ou allaitantes.
- Interactions médicamenteuses et autres formes d'interactions
Aucune information n’est disponible concernant l’innocuité et l’efficacité de ce vaccin lorsqu’il est utilisé avec un autre médicament vétérinaire. Par conséquent, la décision d’utiliser ce vaccin avant ou après un autre médicament vétérinaire doit être prise au cas par cas.
Effets indésirables et surdosage
- Incompatibilité majeure
Ne pas mélanger avec d’autres médicaments vétérinaires à l’exception du solvant fourni pour être utilisé avec le vaccin.
- Effets indésirables
Dans les 4 heures qui suivent la vaccination, une réaction diffuse oedémateuse, pouvant être chaude et/ou douloureuse, apparaît au site d’injection. La réaction est maximale 2-3 jours après la vaccination, avec une taille maximum de 3 cm sur 8 cm. Cet oedème se résorbe complètement dans les 3 semaines et il n’a, normalement, pas d’impact sur l’appétit de l’animal vacciné et ne provoque pas de gêne apparente. La souche vaccinale peut être à l’origine d’une réaction inflammatoire suppurée au site d’injection, entraînant une rupture de la couche superficielle de la muqueuse labiale et une libération de liquide et de cellules inflammatoires. Un léger écoulement opaque s’écoule du site d’injection dans les 3 ou 4 jours qui suivent la vaccination.
Une légère hypertrophie des noeuds lymphatiques rétro-pharyngés et mandibulaires, pouvant être transitoirement douloureuse, peut se produire pendant les quelques jours qui suivent la vaccination.
Dans de très rares cas, un abcès peut se développer au site d’injection ou au niveau des nœuds lymphatiques.
De plus, une augmentation de la température rectale pouvant atteindre 2°C peut survenir le jour de la vaccination. Dans de rares cas, de l’inappétence, de la fièvre, des frissons et des gonflements
oedémateux diffus (par exemple, oedème facial, museau/lèvre supérieure gonflé) peuvent être observés.
Dans de très rares cas, une dépression peut survenir.
La fréquence des effets indésirables est définie en utilisant la convention suivante :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 au cours d’un traitement)
- fréquent (entre 1 et 10 animaux sur 100)
- peu fréquent (entre 1 et 10 animaux sur 1 000)
- rare (entre 1 et 10 animaux sur 10 000)
- très rare (moins d’un animal sur 10 000, y compris les cas isolés).
Posologie
| Espèce(s) | Posologie |
|---|---|
| Vaccination sous-muqueuse avec 0,2 ml de produit reconstitué.
Protocole vaccinal : Primovaccination : chevaux dès l’âge de 4 mois : 2 administrations d’une dose à 4 semaines d’intervalle.
Rappels : Rappels tous les 3 mois pour maintenir la protection.
A partir de la primo-vaccination, la réponse immunitaire initiale se maintient pendant 6 mois. Ainsi, une seule dose vaccinale sera nécessaire pour rétablir l’immunité.
Il est recommandé que tous les chevaux logés dans une même écurie soient vaccinés.
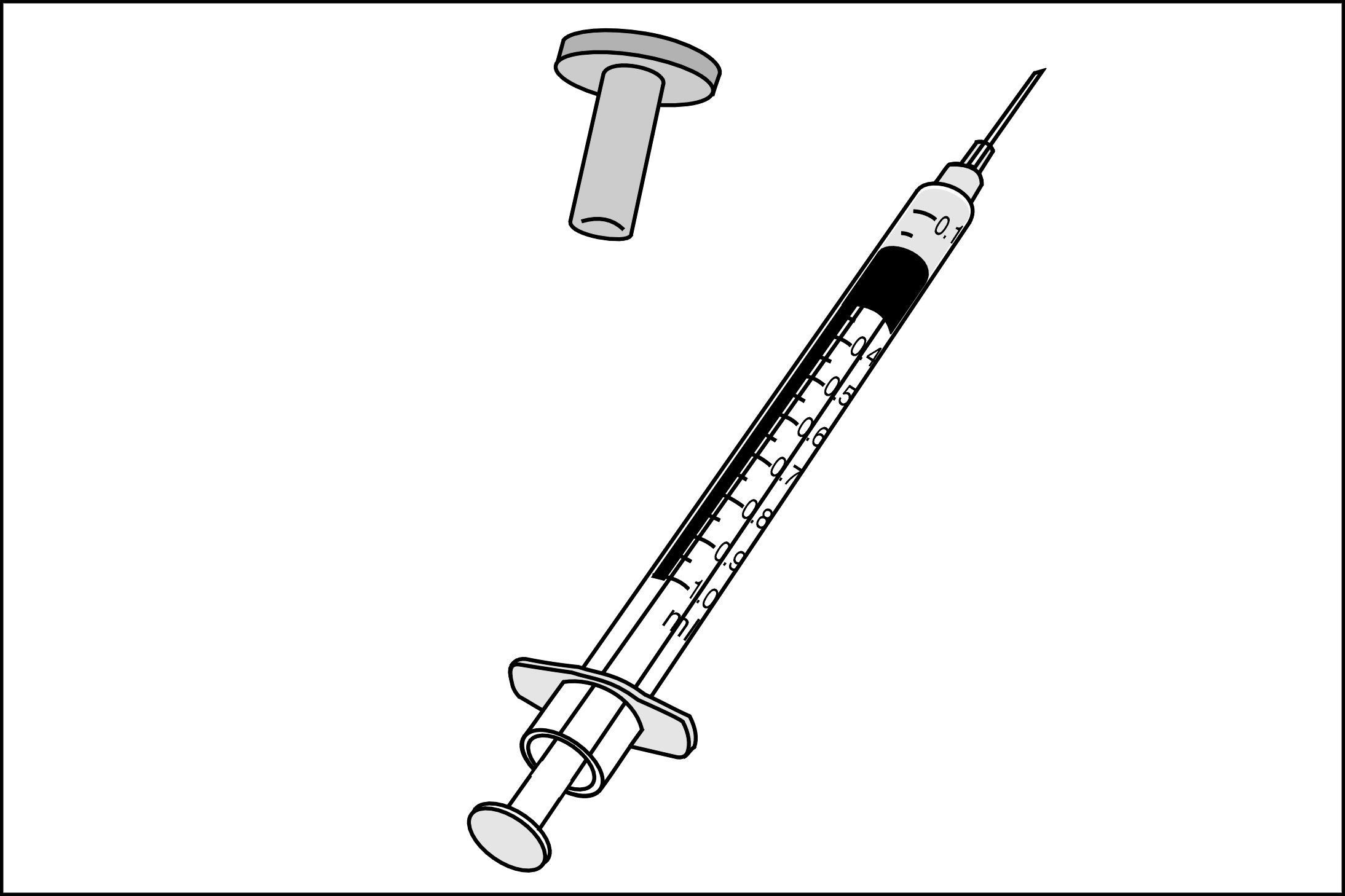
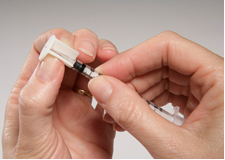
Laisser le solvant stérile atteindre la température ambiante (15-25°C). Reconstituer aseptiquement le lyophilisat avec 0,3 ml du solvant stérile fourni. Laisser le vaccin reconstitué reposer pendant 1 minute et agiter soigneusement pour mélanger le contenu. Ne PAS secouer. Aspirer 0,2 ml du vaccin reconstitué dans la seringue fournie (voir figure 1) et fixer l’embout sur la seringue (voir figure 2).
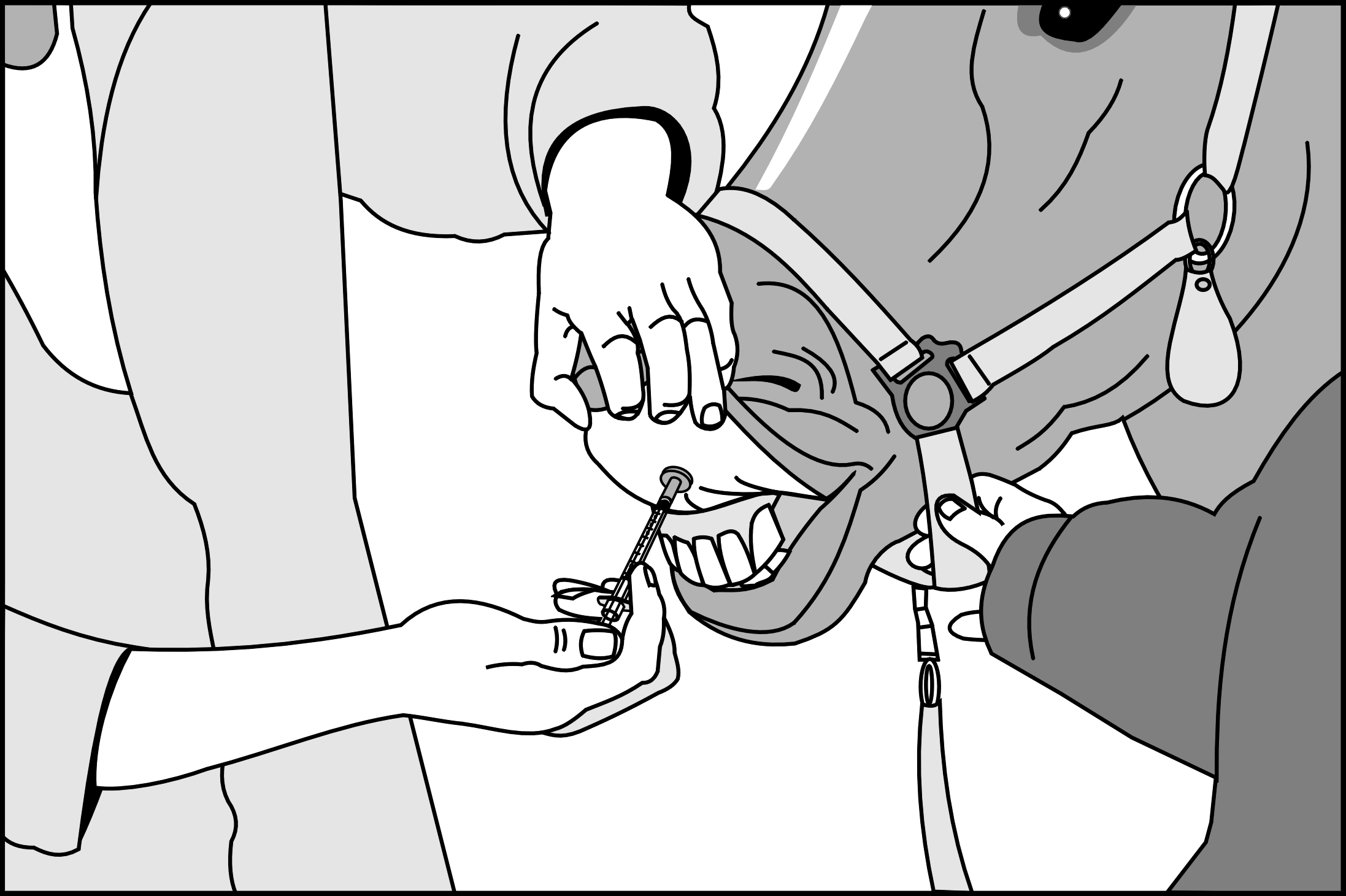
Tenir la tête de l’animal, retourner la lèvre supérieure et piquer l’aiguille dans la lèvre supérieure jusqu’à ce que l’embout bute sur la lèvre. Injecter la totalité du contenu de la seringue dans la lèvre supérieure (voir figure 3).
Figure 1
Figure 2
Figure 3
|
Temps d'attente
- Voie d'administration
Conservation et stockage
- Température de conservation
Lyophilisat : conserver au réfrigérateur (entre +2°C et +8°C). Protéger de la lumière.
Solvant : aucune précaution particulière de conservation.
Tenir hors de la portée et de la vue des enfants
- Précautions particulières de conservation selon pertinence
- Non renseigné
- Précaution particulière à prendre lors de l'élimination
Tous médicaments vétérinaires non utilisés ou déchets dérivés de ces médicaments doivent être éliminés conformément aux exigences locales.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| EQUILIS® Strep E Boîte de 10 flacons de lyophilisat, de 10 flacons de 0,5 mL de solvant et de 10 embouts et 10 seringues avec aiguilles | Oui | Non renseigné | EU/2/04/043/001 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- INTERVET INTERNATIONAL B.V.
- WIM DE KORVERSTRAAT 35
5831 AN BOXMEER
PAYS-BAS
- Responsable de la mise sur le marché
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex
- Responsable de la pharmacovigilance
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex