FinadyneⓇ Transdermal 50 mg/mL solution pour pour-on pour bovins
Identification
- Dénomination du médicament vétérinaire
- FinadyneⓇ Transdermal 50 mg/mL solution pour pour-on pour bovins
- Forme pharmaceutique
- Solution pour Pour-On
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Flunixine (sous forme de méglumine) 50 mg - Excipients
Nom de l'excipient Quantité de l'excipient Lévomenthol 50 mg Rouge allura AC (E129) 0.2 mg Pyrrolidone Dicaprylocaprate de propylène glycol Monocaprylate de glycérol - Informations supplémentaires
Chaque mL contient :
Substance active :
Flunixine ............................................................. 50 mg
(sous forme de méglumine)
(équivalant à 83 mg de flunixine méglumine)
Excipients :
Composition qualitative en excipients et autres composants Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire Lévomenthol
50,0 mg Rouge allura AC (E129)
0,2 mg Pyrrolidone Dicaprylocaprate de propylène glycol
Monocaprylate de glycérol
Liquide rouge clair, limpide et exempt de particules visibles.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| - Réduction de la fièvre associée à une maladie respiratoire bovine. - Réduction de la fièvre associée à des mammites aiguës. - Réduction de la douleur et de la boiterie associées à un phlegmon interdigité (panaris), une dermatite interdigitée (fourchet) et une dermatite digitée (maladie de Mortellaro). |
- Contre-indications
Ne pas administrer aux animaux atteints de maladies cardiaque, hépatique ou rénale, ou s'il existe des signes d'ulcération gastro-intestinale ou de saignement.
Ne pas utiliser chez les animaux atteints de déshydratation sévère, d’hypovolémie car il existe un risque potentiel d’augmentation de toxicité rénale.
Ne pas administrer le médicament vétérinaire aux vaches dans les 48 heures précédant la date prévue de la parturition.
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Appliquer uniquement sur une peau sèche et éviter toute exposition à l’humidité pendant au moins 6 heures après l’application.
En cas d’infection(s) bactérienne(s), un traitement antibiotique concomitant devra être envisagé.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Voir également la rubrique 3.7.
Les anti-inflammatoires non stéroïdiens (AINS) sont connus pour potentiellement retarder la parturition par un effet tocolytique induit par l’inhibition des prostaglandines responsables de l’induction de la parturition. L’utilisation du produit dans la période qui suit la parturition peut interférer avec l’involution utérine et l’expulsion de membranes fœtales, entraînant une rétention placentaire.
Aucune étude d’innocuité n’a été menée chez les taureaux adultes destinés à la reproduction. Les études de laboratoire sur les rats n'ont pas mis en évidence d’effet toxique sur la reproduction. L’utilisation de la spécialité ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
L’utilisation du médicament chez des animaux pré-ruminants et âgés peut entraîner un risque supplémentaire. Si l’utilisation du médicament ne peut pas être évitée, une diminution de la dose et un suivi clinique rigoureux devront être envisagés.
Appliquer uniquement sur une peau saine.
La flunixine est toxique pour les oiseaux nécrophages. Ne pas administrer aux animaux susceptibles d'entrer dans la chaîne alimentaire de la faune sauvage. En cas de mort naturelle ou d’euthanasie d’animaux traités, s’assurer que la faune sauvage n’aura pas accès aux carcasses et ne pourra pas les consommer.
- Précaution particulière à prendre par la personne qui administre le médicament
Les anti-inflammatoires non stéroïdiens (AINS) peuvent occasionner une hypersensibilité (allergie).
Les personnes présentant une hypersensibilité connue aux AINS doivent éviter tout contact avec le médicament vétérinaire.
Il a été démontré que le produit peut provoquer des dommages oculaires graves et irréversibles et une légère irritation cutanée. L'ingestion du produit ou tout contact avec la peau peut être nocif.
Eviter tout contact avec les yeux, incluant le contact des yeux par les mains. Eviter tout contact avec la peau.
Eviter tout contact avec la surface traitée (permettant une diffusion du produit) sans le port de gants de protection, pendant au moins trois jours ou jusqu’à ce que le site d’application soit sec (si le délai est plus long).
Eviter que les enfants aient accès au produit ou aux animaux traités.
Un équipement de protection individuelle consistant en des gants imperméables, des vêtements de protection et des lunettes de sécurité doit être porté lors de la manipulation du médicament vétérinaire.
En cas d’ingestion accidentelle ou de contact avec la bouche, rincez immédiatement et abondamment avec de l’eau, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
En cas de contact avec les yeux, rincez immédiatement et abondamment avec de l’eau propre et demandez conseil à un médecin.
En cas de contact avec la peau, lavez abondamment avec de l’eau et du savon.
Ne pas fumer, manger ou boire lors de la manipulation du produit. Se laver les mains après utilisation.
- Précautions particulières concernant la protection de l'environnement
Sans objet
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation et lactation :
Le produit peut être utilisé pendant la gestation et la lactation, excepté dans les 48 heures qui précèdent la parturition.
En raison du risque accru de rétention placentaire, le produit ne devrait être administré, dans les 36 heures qui suivent la parturition, qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable, et le risque de rétention placentaire devrait être surveillé chez les animaux traités.
- Interactions médicamenteuses et autres formes d'interactions
Ne pas administrer d’autres AINS simultanément, ou à moins de 24 heures d’intervalle.
Certains AINS peuvent être fortement liés aux protéines plasmatiques et être en concurrence avec d’autres médicaments fortement liés, ce qui peut entraîner des effets toxiques. L’administration simultanée de médicaments potentiellement néphrotoxiques doit être évitée.
- Anti-microbiens et anti-parasitaires : lutte contre les résistances
Sans objet.
Effets indésirables et surdosage
- Incompatibilité majeure
En l’absence d’études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d’autres médicaments vétérinaires.
- Effets indésirables
Bovins :
Fréquent
(1 à 10 animaux / 100 animaux traités) :
Gonflement au site d’application1, érythème au site d’application1, peau sèche au site d’application (pellicules)1, changement de l’aspect des poils au site d’application (poils cassés/fragiles, poils plus fins)1, alopécie au site d’application1, épaississement de la peau au site d’application1
Inconfort2 ; Agitation2 ; Irritabilité2
Très rare
(<1 animal / 10 000 animaux traités, y compris les cas isolés) :
Anaphylaxie3 1 Ces changements ont été rapportés comme étant transitoires. En général, aucun traitement spécifique n’est nécessaire.
2 Signes temporaires
3 Peut être grave, peut survenir et doit être traitée de façon symptomatique
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir également la rubrique « Coordonnées » de la notice.
Posologie
| Espèce(s) | Posologie |
|---|---|
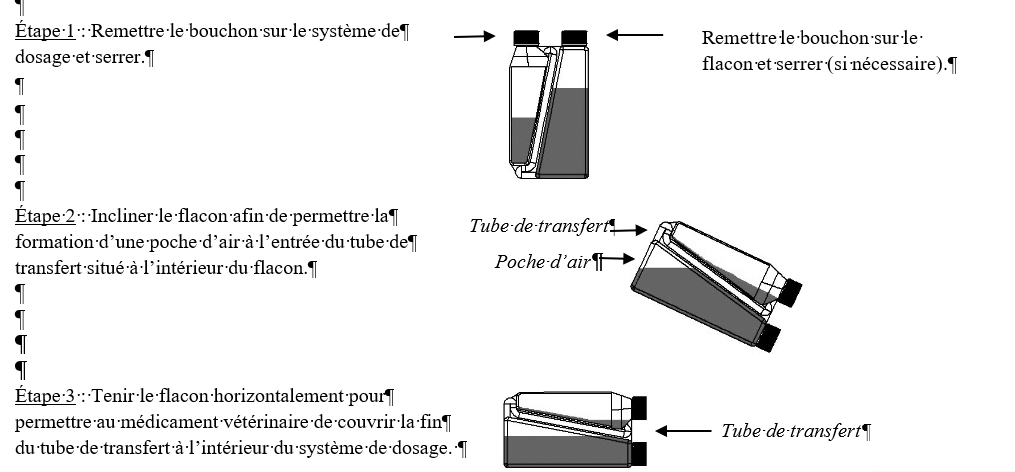
| Usage en pour-on. Application unique. La dose de traitement recommandée est de 3,33 mg de flunixine/kg de poids vif (équivalant à 1 mL/15 kg de poids vif). Le système de dosage du flacon est calibré en kilogrammes de poids vif. Afin de garantir une posologie appropriée, le poids corporel doit être déterminé aussi précisément que possible. Avant de traiter les animaux, tester plusieurs fois les instructions d’administration, afin de se familiariser avec le mode de fonctionnement du système de dosage.
Étape 1 : A la première utilisation, retirer le bouchon et le joint détachable du système de dosage. 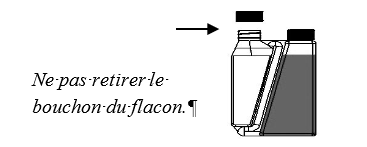
Étape 2 : Tenir le flacon en position verticale au niveau des yeux et presser lentement et doucement le flacon pour remplir le système de dosage jusqu’au niveau sélectionné. Si le système de dosage est trop plein, suivre les Instructions de Réduction du Trop-plein. 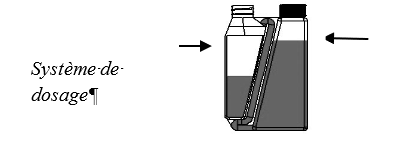
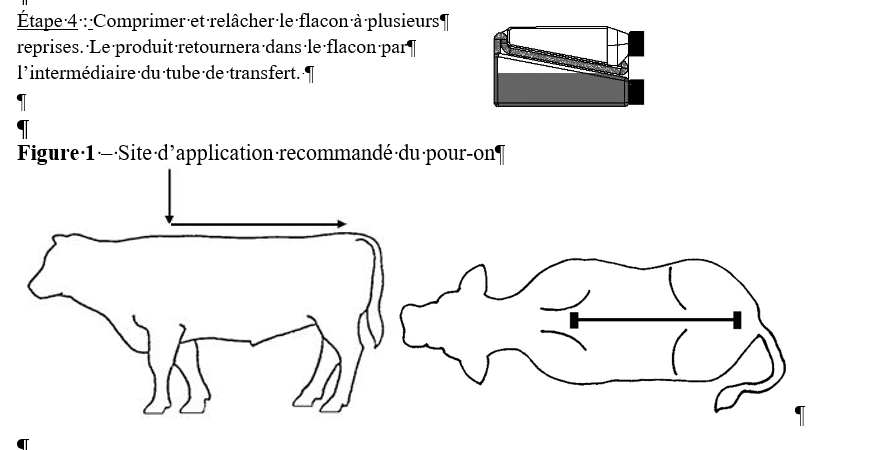
Étape 3 : Verser le volume mesuré le long de la ligne dorsale, à partir du garrot jusqu’à la base de la queue. Une petite quantité de liquide reste le long des parois du système de dosage, mais la calibration de celui-ci en tient compte. Eviter de comprimer le flacon pendant que la solution est versée à partir du système de dosage. 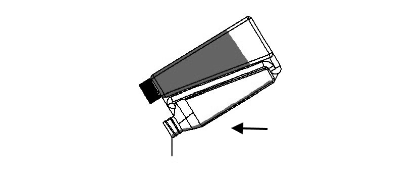
Instructions de réduction du trop-plein
|
Temps d'attente
- Voie d'administration
- Pour-on
Conservation et stockage
- Température de conservation
- Non renseigné
- Précautions particulières de conservation selon pertinence
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
Tenir hors de la vue et de la portée des enfants.- Précaution particulière à prendre lors de l'élimination
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| FINADYNE TRANSDERMAL® 50 mg/mL Boîte de 1 flacon de 250 mL | Non | Soumis à prescription | FR/V/9151586 5/2014 |
| FINADYNE TRANSDERMAL® 50 mg/mL Boîte de 1 flacon de 100 mL | Non | Soumis à prescription | FR/V/9151586 5/2014 |
| FINADYNE TRANSDERMAL® 50 mg/mL Boîte de 1 flacon de 1 litre | Non | Soumis à prescription | FR/V/9151586 5/2014 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex
- Responsable de la mise sur le marché
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex
- Responsable de la pharmacovigilance
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex