ShutOutⓇ suspension intramammaire pour vaches au tarissement
Identification
- Dénomination du médicament vétérinaire
- ShutOutⓇ suspension intramammaire pour vaches au tarissement
- Forme pharmaceutique
- Suspension intramammaire
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Bismuth lourd (sous forme de sous-nitrate) 1.9 g - Excipients
Nom de l'excipient Paraffine liquide Stéarate d'aluminium Silice colloïdale - Informations supplémentaires
Chaque seringue intramammaire de 4 g contient :
Substance active :
Sous-nitrate de bismuth 2,6 g
(équivalant à 1,9 g de bismuth)
Excipients :
Composition qualitative en excipients et autres composants Paraffine liquide Stéarate d’aluminium Silice colloïdale anhydre Suspension homogène, blanche à légèrement jaune.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Prévention de nouvelles infections intramammaires pendant toute la période du tarissement.
Chez les vaches ne présentant vraisemblablement pas de mammite subclinique, le médicament peut être utilisé seul dans le cadre d’un plan de gestion du troupeau au tarissement et de contrôle de mammites. |
- Contre-indications
Ne pas utiliser le médicament vétérinaire seul chez les vaches présentant une mammite subclinique au tarissement.
Ne pas utiliser chez les vaches présentant une mammite clinique au tarissement.
Ne pas utiliser chez les vaches en lactation. Voir la rubrique 3.7.
Ne pas utiliser en cas d'hypersensibilité à la substance active ou à l'un des excipients.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
La sélection des vaches pour le traitement par le médicament vétérinaire doit reposer sur le jugement clinique du vétérinaire.
Les critères de sélection peuvent être basés sur les antécédents de mammite et l’historique des numérations cellulaires individuelles des vaches, ou sur les résultats de tests reconnus pour la détection des mammites subcliniques, ou sur des prélèvements bactériologiques.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Il fait partie des bonnes pratiques de surveiller régulièrement les vaches taries pour déceler tout signe de mammite clinique. Si une mammite clinique se déclare dans un quartier obturé, il est nécessaire de traire manuellement ce quartier avant d’instaurer un traitement approprié.
Afin de réduire le risque de contamination, ne pas immerger la seringue intramammaire dans l’eau.
N'utilisez la seringue qu'une seule fois.
Ce médicament vétérinaire n’ayant pas d’activité antimicrobienne, il est important de respecter une technique aseptique stricte pour l'administration du médicament vétérinaire.
Ne pas administrer d'autre produit intramammaire après l'administration du médicament vétérinaire.
Chez les vaches pouvant présenter une mammite subclinique, le médicament vétérinaire peut être utilisé après administration dans le quartier infecté d’un traitement antibiotique adapté au tarissement.
- Précaution particulière à prendre par la personne qui administre le médicament
Ce médicament vétérinaire peut provoquer une irritation de la peau et des yeux. Éviter tout contact avec la peau ou les yeux.
En cas de contact avec la peau ou les yeux, lavez abondamment la zone affectée à l'eau.
Les sels de bismuth ont été associés à des réactions d'hypersensibilité. Les personnes présentant une hypersensibilité connue aux sels de bismuth, doivent éviter tout contact avec le médicament vétérinaire.
Si vous présentez des symptômes à la suite d'une exposition, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette.
Se laver les mains après utilisation.
Lingettes désinfectantes :
En raison de la présence d’alcool isopropylique, les lingettes désinfectantes peuvent provoquer une irritation de la peau et des yeux.
Eviter le contact avec les yeux. Eviter le contact prolongé avec la peau. Eviter l’inhalation des vapeurs.
Le port de gants peut prévenir une irritation de la peau.
Se laver les mains après utilisation.
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation :
Le médicament vétérinaire n’étant pas absorbé par la glande mammaire, il peut être utilisé chez les vaches gestantes. Au moment du vêlage, le bouchon peut être ingéré par le veau. L’ingestion du médicament vétérinaire par le veau est sans danger et n’entraîne pas d’effets secondaires indésirables.
Lactation :
Le médicament vétérinaire est indiqué chez les vaches laitières au tarissement. En cas d'utilisation accidentelle chez une vache en lactation, une légère augmentation transitoire de la numération
- Interactions médicamenteuses et autres formes d'interactions
Lors des essais cliniques, la compatibilité d’une formulation comparable du médicament a été démontrée seulement avec des produits de tarissement contenant de la cloxacilline.
Voir également la rubrique 3.5.
- Anti-microbiens et anti-parasitaires : lutte contre les résistances
Sans objet.
Effets indésirables et surdosage
- Incompatibilité majeure
Sans objet
- Effets indésirables
Aucun connu.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Voie intramammaire.
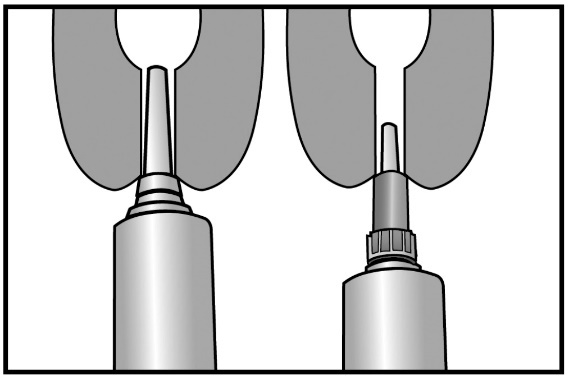
Le médicament vétérinaire est doté d’une tête à double embout. Le capuchon de la seringue peut être partiellement ou totalement retiré. Il est recommandé de pincer le trayon à sa base car cela aide à positionner la pâte dans le canal ou la lumière du trayon, en bouchant le canal du trayon par le haut. Option de l’embout court : L’option de l’embout court donne la possibilité d’une insertion partielle, de sorte que la seringue n’a à être insérée que dans l'extrémité du trayon. Option de l’embout long : L’option de l’embout long peut être utilisée pour faciliter le traitement, par exemple pour éviter que l’embout ne s'affaisse dans le cas d'une vache en mouvement ou nerveuse. Étape 1 : Retrait du capuchon sécable Étape 2 : Insertion de l’embout long ou court
Administrer le contenu d'une seringue dans chaque quartier immédiatement après la dernière traite (tarissement). Ne pas masser le trayon ou la mamelle après infusion du médicament vétérinaire parce qu'il est important que le produit d'étanchéité reste dans le trayon uniquement et ne pénètre pas dans la mamelle.
Veiller à ne pas introduire de germes pathogènes dans le trayon afin de diminuer le risque de mammite après l'administration.
Il est impératif que le trayon soit bien nettoyé et désinfecté avec les lingettes désinfectantes fournies. Nettoyer les trayons jusqu'à ce que les lingettes restent propres. Laisser sécher les trayons avant l'administration. Administrer de manière aseptique en prenant soin de ne pas contaminer l'embout de la seringue. Après l'infusion, il est conseillé d’utiliser un produit de trempage ou un spray.
Par temps froid, le médicament vétérinaire peut être réchauffé à température ambiante dans un environnement chaud pour faciliter son extraction. | ||||||||||||||||||
Temps d'attente
- Voie d'administration
- Intramammaire
Conservation et stockage
- Température de conservation
- Non renseigné
- Précautions particulières de conservation selon pertinence
Ce médicament vétérinaire ne nécessite pas de conditions particulières de conservation.
Tenir hors de la vue et de la portée des enfants.
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| Seau de 144 seringues pour administration intramammaire de 4 g et 144 lingettes nettoyantes | Oui | Non soumis à prescription | FR/V/9588473 6/2020 |
| Boîte de 24 seringues pour administration intramammaire de 4 g et 24 lingettes nettoyantes | Oui | Non soumis à prescription | FR/V/9588473 6/2020 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- INTERVET INTERNATIONAL B.V.
- WIM DE KORVERSTRAAT 35
5831 AN BOXMEER
PAYS-BAS
- Responsable de la mise sur le marché
- INTERVET INTERNATIONAL B.V.
- WIM DE KORVERSTRAAT 35
5831 AN BOXMEER
PAYS-BAS
- Responsable de la pharmacovigilance
- INTERVET
- Rue Olivier de Serres
BP 17144
49071 BEAUCOUZE cedex