CYDECTINE® 10 % LA Solution injectable pour bovins
Identification
- Dénomination du médicament vétérinaire
- CYDECTINE® 10 % LA Solution injectable pour bovins
- Forme pharmaceutique
- Solution injectable
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Moxidectine 100 mg - Excipients
Nom de l'excipient Quantité de l'excipient Alcool benzylique (E1519) 70 mg
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Chez les bovins de 100 à 500 kg :
|
- Contre-indications
Ne pas utiliser chez les animaux de moins de 100 kg de poids vif ou de plus de 500 kg de poids vif. Ne pas injecter le produit par voie intravasculaire. L’injection intravasculaire peut entrainer ataxie, paralysie, convulsions, collapsus et la mort. Pour prévenir toute injection intravasculaire, respecter soigneusement la procédure d’administration décrite en rubrique « Posologie et voie d’administration ».
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Des précautions doivent être prises afin d'éviter les pratiques suivantes car elles augmentent le risque de développement de résistance et peuvent rendre le traitement inefficace :
- usage trop fréquent et répété d'anthelminthiques de la même classe pendant une durée prolongée,
- sous-dosage pouvant être lié à une sous-estimation du poids vif, une mauvaise administration du produit, un manque d'étalonnage du dispositif de dosage (s'il en existe un).
Tous les cas cliniques suspects de résistance aux anthelminthiques doivent faire l'objet d'analyses complémentaires en effectuant les tests appropriés (par exemple le test de réduction de l'excrétion des oeufs dans les fèces). En cas de suspicion forte de résistance à un anthelminthique particulier suite aux tests, un anthelminthique appartenant à une autre classe pharmacologique et présentant un autre mécanisme d'action devrait être utilisé.- Précautions particulières pour une utilisation sûre chez les espèces cibles
Pour éviter les abcès, une asepsie stricte est recommandée.
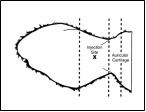
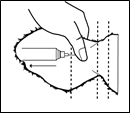
Le médicament a été formulé tout particulièrement pour une injection sous-cutanée dans l'oreille de l'animal et ne doit pas être administré par une autre voie ou à d'autres espèces.
Pour éviter des réactions secondaires dues à la mort des larves d'hypodermes dans l'œsophage ou la colonne vertébrale, il est recommandé d'administrer le médicament à la fin de l'activité des mouches et avant que les larves n'atteignent leur site. Consulter le vétérinaire pour connaître la période correcte de traitement.
L'immunité sur les nématodes dépend d'une bonne exposition. Bien que ce ne soit pas le cas normalement, il peut arriver que des mesures de contrôle antiparasitaires accroissent la vulnérabilité des bovins à la ré-infestation. Les animaux courent des risques de ré-infestation vers la fin de leur première saison de pâture, spécialement si la saison est longue, ou bien l'année suivante, s'ils sont placés sur des pâtures extrêmement contaminées. Des mesures de contrôle complémentaires peuvent alors être envisagées.
- Précaution particulière à prendre par la personne qui administre le médicament
Eviter le contact direct avec la peau et les yeux.
Se laver les mains après usage.
Ne pas fumer, boire ou manger en manipulant le produit.
Veiller à ne pas s'auto-injecter le produit. Consulter un médecin généraliste en cas d'auto-injection accidentelle, traiter tout symptôme particulier.- Précautions particulières concernant la protection de l'environnement
N/A
- Autres précautions
La moxidectine remplit les critères pour être classée comme substance (très) persistante, bioaccumulable et toxique (PBT), par conséquent, l’exposition de l’environnement à la moxidectine doit être limitée autant que possible. Les traitements ne doivent être administrés que lorsque cela est nécessaire et doivent être basés sur le nombre d'œufs présents dans les excréments ou l’évaluation du risque d’infestation au niveau de l’animal et/ou du troupeau.
À l’instar des autres lactones macrocycliques, la moxidectine peut entraîner des effets indésirables pour les organismes non ciblés.
- Les excréments contenant de la moxidectine excrétés dans les prairies par des animaux traités peuvent temporairement réduire l’abondance d’organismes se nourrissant de fumier. Après avoir traité des bovins avec le produit, des niveaux de moxidectine, potentiellement toxiques pour les espèces de mouches du fumier, peuvent être excrétés durant une période de plus de quatre semaines et peuvent réduire l’abondance de mouches du fumier durant cette période. Il a été établi lors d’essais en laboratoire que la moxidectine pouvait affecter temporairement la reproduction des coléoptères coprophages; toutefois, des études sur le terrain ont conclu à l’absence de tout effet sur le long terme. Néanmoins, en cas de traitements répétés avec la moxidectine (tout comme avec les produits de la même classe des anthelminthiques), il est conseillé de ne pas traiter à chaque fois les animaux dans la même prairie afin de permettre aux populations de faune du fumier de se rétablir.
- La moxidectine est intrinsèquement toxique pour les organismes aquatiques, y compris les poissons. Le produit doit uniquement être utilisé conformément aux instructions de l’étiquetage. D’après le profil d’excrétion de la moxidectine lorsqu’elle est administrée sous forme de formulation injectable, les animaux traités ne doivent pas pouvoir accéder aux cours d’eau durant les 10 jours suivant le traitement.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
La spécialité peut être utilisée chez les femelles gravides.
- Interactions médicamenteuses et autres formes d'interactions
Les effets des GABA agonistes sont augmentés par la moxidectine.
Effets indésirables et surdosage
- Incompatibilité majeure
En l’absence d’études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d’autres médicaments vétérinaires.
- Effets indésirables
Dans de rare cas, on peut observer au site d'injection un gonflement immédiat ou retardé qui peuvent dégénérer en abcès (dans environ 1% des cas). La fréquence des gonflements au point d'injection tend à être supérieure chez les animaux plus lourds. Ces effets secondaires disparaissent généralement sans traitement, dans les 14 jours après administration mais certains peuvent persister jusqu'à 5 semaines chez certains animaux (< 5 %) et plus longtemps dans de très rares cas.
On peut observer dans de rares cas ataxie et dépression après injection.
En cas de réaction d'hypersensibilité, traiter les signes cliniques de manière symptomatique.
La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
Posologie
| Espèce(s) | Posologie | ||||||
|---|---|---|---|---|---|---|---|
| 1 mg de moxidectine par kg de poids vif soit 0,5 mL de solution pour 50 kg de poids vif, en une injection unique par voie sous-cutanée à l'oreille en utilisant une aiguille hypodermique de G18 25-40 mm. Utiliser une seringue automatique pour le flacon de 200 mL.
|
Temps d'attente
- Voie d'administration
- Sous-cutanée
Conservation et stockage
- Température de conservation
Ne pas conserver à une température supérieure à 25°C.
Conserver à l'abri de la lumière.- Précautions particulières de conservation selon pertinence
- Non renseigné
- Précaution particulière à prendre lors de l'élimination
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets. Le produit ne doit pas être déversé dans les cours d’eau. Extrêmement dangereux pour les poissons et les organismes aquatiques.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| CYDECTINE® 10 % LA Solution injectable pour bovins Boîte de 1 flacon de 200 mL | Oui | Soumis à prescription | FR/V/5341056 8/2005 |
| CYDECTINE® 10 % LA Solution injectable pour bovins Boîte de 1 flacon de 50 mL | Oui | Soumis à prescription | FR/V/5341056 8/2005 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- ZOETIS France
- 107 AVENUE DE LA REPUBLIQUE
92320 CHATILLON
Zoetis Assistance 0800 73 00 65http://www.zoetis.fr
- Responsable de la mise sur le marché
- ZOETIS France
- 107 AVENUE DE LA REPUBLIQUE
92320 CHATILLON
Zoetis Assistance 0800 73 00 65http://www.zoetis.fr
- Responsable de la pharmacovigilance
- ZOETIS France
- 107 AVENUE DE LA REPUBLIQUE
92320 CHATILLON
Zoetis Assistance 0800 73 00 65http://www.zoetis.fr