SEDATOR® Solution injectable
Identification
- Dénomination du médicament vétérinaire
- SEDATOR® Solution injectable
- Forme pharmaceutique
- Solution
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Médétomidine (sous forme de chlorhydrate) 0.85 mg - Excipients
Nom de l'excipient Quantité de l'excipient Parahydroxybenzoate de méthyle (E218) 1 mg Parahydroxybenzoate de propyle (E216) 0.2 mg Chlorure de sodium Acide chlorhydrique (pour l’ajustement du pH) Hydroxyde de sodium (pour l’ajustement du pH) Eau pour préparations injectables - Informations supplémentaires
Solution aqueuse stérile, claire et incolore.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Chez les chiens et les chats : Sédation en vue de faciliter la manipulation des animaux lors d'examens. Prémédication à une anesthésie générale.
Chez les chats : Anesthésie générale pour des interventions chirurgicales mineures et de courte durée, en association avec la kétamine. |
- Contre-indications
Ne pas utiliser chez les animaux présentant :
- une maladie cardiovasculaire sévère, une maladie respiratoire ou des troubles hépatiques ou rénaux,
- des troubles mécaniques du tractus gastro-intestinal (torsion de l'estomac, incarcérations, obstructions de l'œsophage),
- un diabète sucré,
- un état de choc, ou chez des animaux émaciés ou sévèrement débilités.
Ne pas administrer d'amines sympathomimétiques de manière concomitante.
Ne pas utiliser en cas d'hypersensibilité connue à la substance active ou à l'un des excipients.
Ne pas utiliser chez les animaux souffrant de problèmes oculaires pour lesquels une augmentation de la pression intra-oculaire serait préjudiciable.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
La médétomidine peut ne pas procurer une analgésie durant toute la période de sédation.
Le recours à des moyens analgésiques supplémentaires devra être étudiés lors d'interventions chirurgicales douloureuses.- Précautions particulières pour une utilisation sûre chez les espèces cibles
Un examen clinique sera pratiqué sur tous les animaux avant l'utilisation de médicaments vétérinaires destinés à la sédation et/ou l'anesthésie générale.
Il convient d'éviter des doses plus élevées de médétomidine chez les chiens de grande race.
Il convient d'être prudent en cas d'association de médétomidine avec d'autres anesthétiques ou sédatifs (kétamine, thiopental, halothane, propofol par exemple) en raison de ses effets potentialisateurs marqués de l'anesthésie.
La posologie de l'anesthésique sera réduite en proportion et titrée en fonction de la réaction de l'animal, en raison de la variabilité considérable des réponses entre les animaux. Avant de procéder à toute association, il convient de respecter les mises en garde et contre-indications figurant dans la littérature relative aux autres médicaments vétérinaires.
Les animaux doivent être à jeun 12 heures avant l'anesthésie.
L'animal doit être placé dans un environnement calme et tranquille afin de permettre à la sédation d'atteindre son effet maximum. Cela prend environ 10 – 15 minutes. Il convient de ne pas débuter d'intervention ou d'administrer d'autres médicaments avant obtention de la sédation maximum.
Les animaux traités seront gardés au chaud et à température constante, pendant l'intervention et au réveil. Les yeux seront protégés par un lubrifiant approprié.
Il convient de donner aux animaux nerveux, agressifs ou excités la possibilité de se calmer avant le début du traitement.
Les chiens et chats malades et débilités seront prémédiqués uniquement à la médétomidine avant l'induction et la maintenance d'une anesthésie générale basée sur une évaluation du rapport bénéfice/risque.
On utilisera la médétomidine avec prudence chez les animaux souffrant d'une maladie cardiovasculaire, âgés ou en mauvaise condition générale. Les fonctions hépatiques et rénales seront évaluées avant l'utilisation du médicament.
La médétomidine peut provoquer une dépression respiratoire; en pareil cas, une ventilation manuelle et une administration d'oxygène peuvent être réalisées.
Afin de réduire le temps de réveil après anesthésie ou sédation, l'effet du médicament peut être désactivé par l'administration d'un alpha-2 antagoniste, l'atipamézole ou la yohimbine par exemple. Comme la kétamine est susceptible de provoquer des crampes, il convient de ne pas administrer les alpha-2 antagonistes avant 30-40 min. après l'administration de kétamine. Cf rubrique 3.10 pour les instructions de posologie.
- Précaution particulière à prendre par la personne qui administre le médicament
En cas d'auto-injection ou d'ingestion accidentelles, demandez immédiatement conseil à un médecin et montrez-lui la notice ou l’étiquette. Cependant, NE CONDUISEZ PAS car le produit peut entraîner une sédation et une modification de la tension artérielle.
Éviter tout contact avec la peau, les yeux ou les muqueuses.
En cas d'exposition cutanée, rincer immédiatement et abondamment à l'eau claire.
Enlever les vêtements contaminés en contact direct avec la peau.
En cas de contact accidentel avec les yeux, rincer abondamment à l'eau claire. En cas d'apparition de symptômes, consulter un médecin.
Les femmes enceintes manipulant le médicament vétérinaire prendront particulièrement garde à ne se pas se l'auto-injecter. Des contractions utérines et une baisse de la tension artérielle chez le fœtus peuvent survenir à la suite d'une exposition systémique accidentelle.
Pour le médecin : la médétomidine est un agoniste des récepteurs alpha-2-adrénergiques. Les symptômes après absorption peuvent comprendre des signes cliniques, tels que : sédation dose-dépendante, dépression respiratoire, bradycardie, hypotension, bouche sèche et hyperglycémie. Des arythmies ventriculaires ont également été rapportées. Les symptômes respiratoires et hémodynamiques doivent recevoir un traitement symptomatique.
- Précautions particulières concernant la protection de l'environnement
Aucune.
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation et de lactation.
Ne pas utiliser durant la gestation et la lactation.
- Interactions médicamenteuses et autres formes d'interactions
L’administration concomitante d’autres dépresseurs du système nerveux central peut potentialiser l’effet de chacune des substances actives. Il convient d’adapter spécifiquement la posologie. La médétomidine a un effet potentialisateur marqué sur les anesthésiques.
Les effets de la médétomidine peuvent être antagonisés par l’administration d’atipamézole ou de yohimbine.
Effets indésirables et surdosage
- Incompatibilité majeure
En l’absence d’études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d’autres médicaments vétérinaires dans la même seringue.
- Effets indésirables
Chiens et chats :
Rare
(1 à 10 animaux / 10 000 animaux traités) :
Œdème pulmonaire Très rare
(< 1 animal / 10 000 animaux traités, y compris les cas isolés) :
Bradycardie, bloc cardiaque du 1er degré, bloc cardiaque du 2e degré, extrasystoles, hypertension a, diminution du débit cardiaque, dépression cardiovasculaire b
Dépression respiratoire b
Cyanose, hypothermie
Vomissements c
Sensibilité accrue aux bruits, tremblements musculaires
Polyurie
Hyperglycémie d
Douleur au site d’injection
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) : Vasoconstriction de l’artère coronaire a Augmentation de la tension artérielle suite à l’administration du médicament, puis retour à la normale, ou légèrement en dessous de la normale.
b Une ventilation manuelle et une administration d’oxygène peuvent être indiquées. L’atropine peut augmenter la fréquence cardiaque.
c Surviennent chez certains chiens et la plupart des chats dans les 5 à 10 minutes après l’injection, et aussi au réveil chez les chats.
d Réversible, due à une dépression de la sécrétion d’insuline.
Les chiens dont le poids est inférieur à 10 kg peuvent davantage présenter les effets indésirables mentionnés ci-dessus.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
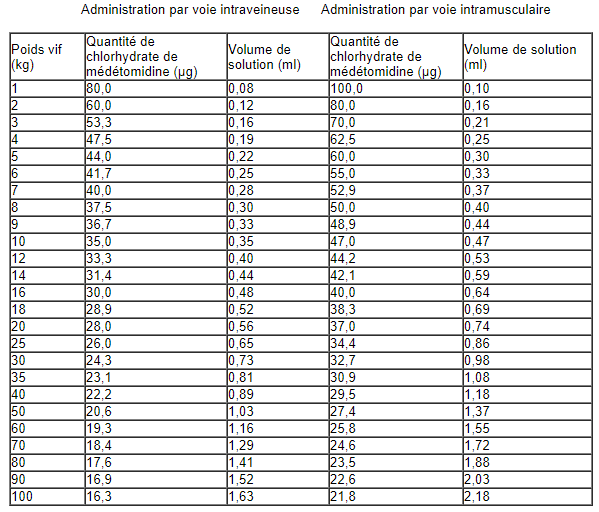
| Espèce(s) | Posologie |
|---|---|
| L’utilisation d’une seringue convenablement graduée est recommandée afin d’assurer un dosage précis lors de l’administration de petits volumes.
|
Temps d'attente
- Voie d'administration
- Intraveineuse
- Intramusculaire
Conservation et stockage
- Température de conservation
Ne pas congeler.
- Précautions particulières de conservation selon pertinence
En cas d’ingestion ou d’auto-injection accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice. Cependant, NE CONDUISEZ PAS, car le produit peut entraîner une sédation et une modification de la tension artérielle.
En cas de contact accidentel du produit avec les yeux, rincer abondamment à l’eau claire. En cas d’apparition de symptômes, consulter un médecin.
Les femmes enceintes manipulant le produit prendront particulièrement garde à ne pas se l’auto-injecter. Des contractions utérines et une baisse de la tension artérielle chez le fœtus peuvent survenir à la suite d’une exposition systémique accidentelle.- Précaution particulière à prendre lors de l'élimination
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation des déchets.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| SEDATOR® Solution injectable Boîte de 1 flacon de 10 mL | Oui | Administration exclusivement réservée aux vétérinaires | FR/V/3786694 3/2007 |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- EUROVET ANIMAL HEALTH
- HANDELSWEG 25 5531 AE BLADEL PAYS-BAS
- Responsable de la mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la pharmacovigilance
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX01.30.48.71.40
https://www.dechra.fr/