TRALIEVE® 70,3 mg Comprimés à croquer pour chiens
Identification
- Dénomination du médicament vétérinaire
- TRALIEVE® 70,3 mg Comprimés à croquer pour chiens
- Forme pharmaceutique
- Comprimé
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Tramadol (sous forme de chlorhydrate) 70.3 mg
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Réduction des douleurs aiguës et chroniques d’intensité légère au niveau des tissus mous et du système musculo-squelettique. |
- Contre-indications
Ne pas administrer en même temps que des antidépresseurs tricycliques, des inhibiteurs de la monoamine oxydase ou des inhibiteurs de la recapture de la sérotonine.
Ne pas utiliser en cas d’hypersensibilité au tramadol ou à l’un des excipients.
Ne pas utiliser chez les animaux atteints d'épilepsie.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
Les effets analgésiques du chlorhydrate de tramadol peuvent être variables. Cette variabilité serait due à des différences individuelles au niveau du métabolisme du médicament qui aboutit au métabolite actif principal, le O-desmethyltramadol. Chez certains chiens (ne répondant pas au traitement), le Les effets analgésiques du chlorhydrate de tramadol peuvent être variables. Cette variabilité serait due à des différences individuelles au niveau du métabolisme du médicament qui aboutit au métabolite actif principal, le O-desmethyltramadol. Chez certains chiens (ne répondant pas au traitement), le médicament vétérinaire peut ainsi ne pas produire l'effet analgésique souhaité. En cas de douleurs chroniques, une analgésie multimodale devra être envisagée. Les chiens doivent donc faire l'objet d'une surveillance régulière par un vétérinaire afin de s'assurer que l'efficacité est suffisante. En cas de réapparition des douleurs ou d’analgésie insuffisante, il pourra être nécessaire de réétudier le protocole analgésique.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
Utiliser avec précaution chez les chiens présentant une insuffisance rénale ou hépatique. Chez les chiens présentant une insuffisance hépatique, le métabolisme du tramadol conduisant à la formation des métabolites actifs peut être réduit, ce qui peut diminuer l’efficacité du médicament vétérinaire. L’un des métabolites actifs du tramadol étant excrété par voie rénale, il peut être nécessaire d’ajuster la posologie chez les chiens présentant une insuffisance rénale. La fonction rénale et la fonction hépatique doivent être surveillées lors de l’utilisation de ce médicament vétérinaire. L’arrêt d’un traitement analgésique de longue durée lorsque cela est possible.
- Précaution particulière à prendre par la personne qui administre le médicament
Les personnes présentant une hypersensibilité connue au tramadol ou à l’un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Le tramadol peut provoquer une sédation, des nausées et des étourdissements en cas d’ingestion accidentelle, en particulier chez les enfants. Afin d’éviter toute ingestion accidentelle, en particulier par un enfant, les morceaux de comprimés inutilisés doivent être replacés dans l’alvéole ouverte de la plaquette et rangés dans la boîte, qui sera conservée en lieu sûr, hors de la vue et de la portée des enfants, car leur ingestion accidentelle pourrait mettre en danger la santé des jeunes enfants. En cas d’ingestion accidentelle, en particulier par des enfants, demander conseil à un médecin et montrez-lui la notice ou l’étiquette. En cas d’ingestion accidentelle par un adulte : NE PAS CONDUIRE car des effets sédatifs sont possibles.
Se laver les mains après utilisation.
- Précautions particulières concernant la protection de l'environnement
Aucune.
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation :
Les études de laboratoire sur les souris et/ou les rats et les lapins n’ont pas mis en évidence d’effets tératogènes, fœtotoxiques, maternotoxiques. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Lactation :
Les études de laboratoire sur les souris et/ou les rats et les lapins n’ont pas mis en évidence d’effets délétères sur le développement périnatal ou postnatal de la progéniture. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
Fertilité :
Lors des études de laboratoire sur les souris et/ou les rats et les lapins, l’utilisation du tramadol aux doses thérapeutiques n’a pas eu d’effet délétère ni sur les performances reproductives, ni sur la fertilité des mâles et des femelles. L’utilisation ne doit se faire qu’après évaluation du rapport bénéfice/risque établie par le vétérinaire responsable.
- Interactions médicamenteuses et autres formes d'interactions
L’administration du médicament vétérinaire en même temps que des dépresseurs du système nerveux central (SNC) pourrait potentialiser les effets dépresseurs sur le SNC et l’appareil respiratoire.
Le tramadol peut amplifier les effets des médicaments qui abaissent le seuil épileptogène.
Les médicaments ayant un effet inhibiteur (cimétidine et érythromycine, par exemple) ou inducteur (carbamazépine, par exemple) sur le métabolisme lié au cytochrome P450 peuvent influer sur l’effet analgésique du tramadol. Les implications cliniques de ces interactions n’ont pas été étudiées chez le chien.
L’administration concomitante d’agonistes/antagonistes mixtes (buprénorphine, butorphanol, par exemple) et de tramadol n’est pas conseillée car l’effet analgésique d’un agoniste pur pourrait en théorie être réduit en pareille circonstance.
Voir également la rubrique 3.3.
Effets indésirables et surdosage
- Incompatibilité majeure
Sans objet.
- Effets indésirables
Chiens :
Fréquent
(1 à 10 animaux / 100 animaux traités) :
Sédationa,b, somnolencesb Peu fréquent
(1 à 10 animaux / 1 000 animaux traités) :
Nausées, vomissements Rare
(1 à 10 animaux / 10 000 animaux traités) :
Réaction d’hypersensibilitéc Très rare
( < 1 animal / 10 000 animaux traités, y compris les cas isolés) :
Convulsionsd a Légère.
b En particulier si les doses administrées sont élevées.
c Le traitement doit être interrompu.
d Chez les chiens présentant un seul épileptogène bas.
Il est important de notifier les effets indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
La dose recommandée est de 2 à 4 mg de chlorhydrate de tramadol par kg de poids corporel toutes les 8 heures ou selon les besoins, en fonction de l’intensité des douleurs. Les doses doivent être espacées de 6 heures au minimum. La dose quotidienne maximale recommandée est de 16 mg/kg. La réponse au tramadol étant variable selon l’individu et dépendant en partie de la posologie, de l’âge de l’animal, des différences individuelles de sensibilité à la douleur et de l’état général de l’animal, la posologie optimale devra être définie au cas par cas en s’appuyant sur les plages de dose et les fréquences de renouvellement indiquées ci-dessus. Le chien devra être examiné régulièrement par un vétérinaire afin de déterminer si une analgésie supplémentaire est nécessaire. L’analgésie supplémentaire pourra être obtenue en augmentant la dose de tramadol jusqu’à atteindre la dose quotidienne maximale et/ou en adoptant une approche multimodale au moyen de l’ajout d’autres analgésiques adéquats. Les comprimés les plus adaptés devront être utilisés afin de limiter autant que possible les comprimés divisés à conserver jusqu’à l’administration suivante.
Le tableau posologique ci-dessous est un guide pour l’administration du médicament vétérinaire à la limite supérieure de la plage de doses : 4 mg/kg de poids corporel. Il indique donc le nombre de comprimés à administrer pour une dose de 4 mg de chlorhydrate de tramadol par kg de poids corporel.
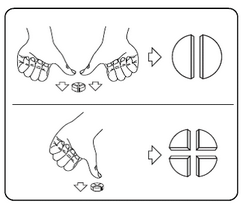
Les comprimés peuvent être divisés en 2 ou 4 parties égales pour assurer le dosage précis. Placer le comprimé sur une surface plane, avec la face portant la barre de sécabilité tournée vers le haut et la face convexe (arrondie) tournée vers le plan de travail.
Division en 2 parties égales : appuyez avec vos pouces des deux côtés du comprimé. Division en 4 parties égales : appuyez avec votre pouce au centre du comprimé. |
Temps d'attente
- Voie d'administration
- Orale
Conservation et stockage
- Température de conservation
À conserver à une température ne dépassant pas 30°C.
À conserver dans l’emballage d’origine de façon à le protéger de l’humidité.
- Précautions particulières de conservation selon pertinence
Le tramadol peut provoquer une sédation, des nausées et des étourdissements en cas d’ingestion accidentelle, en particulier chez les enfants. Afin d’éviter toute ingestion accidentelle, en particulier par un enfant, les morceaux de comprimés inutilisés doivent être replacés dans l’alvéole ouverte de la plaquette et rangés dans la boîte, qui sera conservée en lieu sûr, hors de la vue et de la portée des enfants, car leur ingestion accidentelle pourrait mettre en danger la santé des jeunes enfants. En cas d’ingestion accidentelle, en particulier par des enfants, demander conseil à un médecin et lui montrer la notice ou l’étiquette. En cas d’ingestion accidentelle par un adulte : NE PAS CONDUIRE car des effets sédatifs sont possibles.
Les personnes présentant une hypersensibilité connue au tramadol ou à l’un des excipients doivent éviter tout contact avec le médicament vétérinaire.
Se laver les mains après utilisation.
- Précaution particulière à prendre lors de l'élimination
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| TRALIEVE® 70,3 mg Boîte de 10 plaquettes de 10 comprimés à croquer quadrisécables | Oui | Soumis à prescription | DECHRA REGULATORY B.V. |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la pharmacovigilance
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX01.30.48.71.40
https://www.dechra.fr/