BIMACOX 2,5 MG/ML SUSPENSION BUVABLE POUR AGNEAUX ET VEAUX
Identification
- Dénomination du médicament vétérinaire
- BIMACOX 2,5 MG/ML SUSPENSION BUVABLE POUR AGNEAUX ET VEAUX
- Forme pharmaceutique
- Suspension buvable
Composition
- Principes actifs
- Diclazuril
- Excipients
- Informations supplémentaires
Composition qualitative en excipients et autres composants Composition quantitative si cette information est essentielle à une bonne administration du médicament vétérinaire Parahydroxybenzoate de méthyle (E218) 1,8 mg Parahydroxybenzoate de propyle 0,2 mg Cellulose microcristalline et carmellose sodique / Acide citrique monohydraté / Polysorbate 20 / Hydroxyde de sodium (pour l’ajustement du pH) / Eau purifiée / Suspension homogène de couleur blanche à blanc cassé.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Prévention des signes cliniques des coccidioses dues à Eimeria bovis et Eimeria zuernii. |
| Prévention des signes cliniques des coccidioses dues à Eimeria crandallis et Eimeria ovinoidalis. |
- Contre-indications
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
En l’absence d’antécédents récents et confirmés de coccidiose clinique, il convient de vérifier la présence d’infection coccidienne dans le troupeau avant le traitement.
L’épidémiologie connue d’Eimeria spp. détermine le moment idéal pour le traitement, celui-ci étant le plus efficace pendant la période prépatente de l’infection, avant l’apparition des signes cliniques.
Veaux: Dans certains cas, seule une réduction temporaire de l’excrétion des oocystes peut être obtenue.
Les cas cliniques suspects de résistance aux anticoccidiens doivent faire l'objet d'analyses complémentaires en effectuant les tests appropriés (par exemple le test de réduction de l'excrétion des œufs dans les fèces). En cas de forte suspicion de résistance à un antiprotozoaire particulier suite aux tests, un anticoccidien appartenant à une autre classe pharmacologique et présentant un autre mécanisme d'action devrait être utilisé.
La résistance croisée entre le toltrazuril et le diclazuril est possible et doit être étudiée. Si un test de sensibilité révèle une résistance aux dérivés de la triazine, il convient d’envisager sérieusement de ne pas recourir au diclazuril, car son efficacité peut être réduite.
- Précautions particulières pour une utilisation sûre chez les espèces cibles
L’utilisation du médicament vétérinaire doit être basée sur l’identification et les tests de sensibilité du(des) pathogène(s) cible(s). Si cela n’est pas possible, le traitement doit être basé sur des informations épidémiologiques et sur la connaissance de la sensibilité des agents pathogènes cibles au sein de l’exploitation ou au niveau local/régional.
L’utilisation du médicament vétérinaire doit être conforme aux politiques officielles, nationales et régionales concernant les antimicrobiens.
La coccidiose témoigne d’une hygiène insuffisante au sein d’un troupeau ou d’un enclos. Il est recommandé d’améliorer l’hygiène et de traiter tous les agneaux ou veaux faisant partie d’un même troupeau ou enclos afin de réduire les risques d’infection et d’assurer un meilleur contrôle épidémiologique de la coccidiose.
Pour modifier l’évolution d’une coccidiose clinique établie, il est essentiel de mettre en place une fluidothérapie chez les animaux qui présentent déjà des signes de diarrhée.
L’utilisation préventive de ce médicament vétérinaire doit se limiter aux animaux exposés à un risque très élevé d’infection.
L’utilisation fréquente et répétée d’antiprotozoaires peut entraîner une résistance chez le parasite cible.
- Précaution particulière à prendre par la personne qui administre le médicament
Se laver les mains après l’administration du médicament.
- Précautions particulières concernant la protection de l'environnement
Sans objet.
- Autres précautions
Sans objet.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Sans objet.
- Interactions médicamenteuses et autres formes d'interactions
Aucune connue.
- Anti-microbiens et anti-parasitaires : lutte contre les résistances
Ce médicament est un antiparasitaire. Toute utilisation d’antiparasitaire a un impact potentiel sur les résistances des parasites et sur l’environnement.
Utilisez ce médicament selon les recommandations du Résumé des Caractéristiques du Produit (cf. www.ircp.anmv.anses.fr/).
Effets indésirables et surdosage
- Surdosage (symptômes, conduite d'urgence, antidote)
- Incompatibilité majeure
En l’absence d'études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d’autres médicaments vétérinaires.
- Effets indésirables
Ovins (agneaux) et bovins (veaux) :
Très rare
(< 1 animal / 10 000 animaux traités, y compris les cas isolés):
Troubles de l’appareil digestif (par exemple, diarrhée1,2);
Léthargie, décubitus;
Agitation;
Signes neurologiques (par exemple parésie)
1 avec présence possible de sang
2 chez certains animaux traités, même si l’excrétion des oocystes est réduite à un niveau très faible.
Il est important de notifier les événements indésirables. La notification permet un suivi continu de l’innocuité d’un médicament vétérinaire. Les notifications doivent être envoyées, de préférence par l’intermédiaire d’un vétérinaire, soit au titulaire de l’autorisation de mise sur le marché ou à son représentant local, soit à l’autorité nationale compétente par l’intermédiaire du système national de notification. Voir la notice pour les coordonnées respectives.
Posologie
| Espèce(s) | Posologie |
|---|---|
| Voie orale. Bien agiter avant utilisation. L’utilisation d’un équipement de mesure convenablement étalonné est recommandée pour garantir une posologie précise. Ceci est particulièrement important lors de l’administration de petits volumes. Afin de garantir une posologie appropriée, le poids doit être déterminé aussi précisément que possible. Si les animaux doivent être traités collectivement plutôt qu’individuellement, il convient de les regrouper par poids vif et d’administrer la dose correspondante afin d’éviter les sous- ou les surdosages. 1 mg de diclazuril par kg de poids vif (soit 1 mL de médicament vétérinaire pour 2,5 kg), en une administration orale unique.
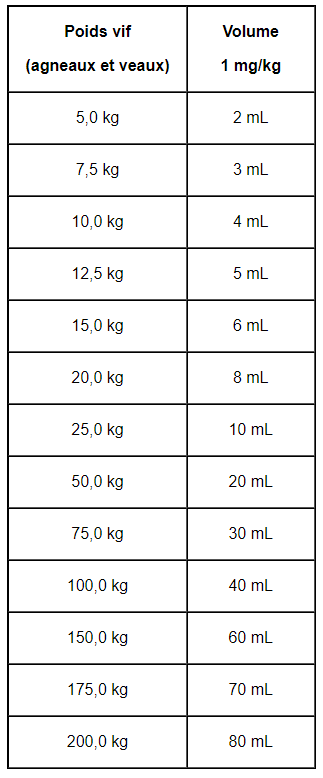 Administrer la suspension buvable directement dans la bouche à l’aide d’un dispositif d’administration adapté. |
Temps d'attente
| Espèce(s) | Denrée | Temps d'attente | Voie d'administration |
|---|---|---|---|
|
| 0.00000 Jour | |
|
| 0.00000 Jour |
Conservation et stockage
- Température de conservation
- Non renseigné
- Précautions particulières de conservation selon pertinence
- Non renseigné
- Précaution particulière à prendre lors de l'élimination
Ne pas jeter les médicaments dans les égouts ou dans les ordures ménagères.
Utiliser les dispositifs de reprise mis en place pour l’élimination de tout médicament vétérinaire non utilisé ou des déchets qui en dérivent, conformément aux exigences locales et à tout système national de collecte applicable au médicament vétérinaire concerné.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| Flacon de 5 L | Non | Soumis à prescription | FR/V/0859546 1/2024 |
| Flacon de 2,5 L | Non | Soumis à prescription | FR/V/0859546 1/2024 |
| Flacon de 1 L | Non | Soumis à prescription | FR/V/0859546 1/2024 |
Informations de révision
- Date de révision de la notice
Responsabilités
- Responsable (Titulaire de l'autorisation de mise sur le marché)
- BIMEDA ANIMAL HEALTH
- Responsable (Responsable de la mise sur le marché)
- BIMEDA France
- Responsable (Responsable de la pharmacovigilance)
- BIMEDA France
