MIRATAZ® 20 mg/g Pommade transdermique pour chats
Identification
- Dénomination du médicament vétérinaire
- MIRATAZ® 20 mg/g Pommade transdermique pour chats
- Forme pharmaceutique
- Pommade
Composition
- Principes actifs
Nom du principe actif Quantité de principe actif Mirtazapine (sous forme d'hémihydrate) 2 mg - Excipients
Nom de l'excipient Quantité de l'excipient Butylhydroxytoluène (E321) 0.01 mg macrogol 400 macrogol 3350 Ether monoéthylique de diéthylèneglycol Macroglycérides caprylocapriques Alcool oléique Butylhydroxytoluène (E321) Diméticone Amidon de tapioca et polyméthylsilsesquioxane - Informations supplémentaires
Pommade transdermique.
Pommade non grasse, homogène, de couleur blanche à blanc cassé.
Usage clinique
Indications d'utilisation par espèce
| Espèce(s) | Utilisation |
|---|---|
| Pour favoriser la prise de poids chez les chats présentant un manque d’appétit et une perte de poids résultant d’une affection chronique. |
- Contre-indications
Ne pas utiliser chez les chats destinés à la reproduction, ni chez les chattes gestantes ou allaitantes. Ne pas utiliser chez les animaux âgés de moins de 7,5 mois ou pesant moins de 2 kg.
Ne pas utiliser en cas d’hypersensibilité à la substance active ou à l’un des excipients.
Ne pas utiliser chez les chats traités avec de la cyproheptadine, du tramadol ou des inhibiteurs de la monoamine oxydase (IMAO) ou ayant été traités avec un IMAO dans les 14 jours précédant le traitement avec le médicament vétérinaire car il peut y avoir une augmentation du risque de syndrome sérotoninergique.
Précautions et mises en garde
- Mise en garde particulière à chaque espèce cible
L’efficacité du médicament vétérinaire n’a pas été établie chez les chats âgés de moins de 3 ans.
L’efficacité et l’innocuité du médicament vétérinaire n’ont pas été établies chez les chats atteints d’une maladie rénale grave et/ou de néoplasie.
Un diagnostic et un traitement appropriés de la maladie sous-jacente sont essentiels à la prise en charge d’une perte de poids, et les options thérapeutiques dépendent de la gravité de la perte de poids et de la ou des maladies sous-jacentes. La prise en charge de toute maladie chronique associée à une perte de poids devrait inclure une nutrition appropriée et une surveillance du poids corporel et de l’appétit.
Le traitement par la mirtazapine ne doit pas remplacer les diagnostics et/ou les traitements nécessaires à la prise en charge de la ou des maladies sous-jacentes qui entraînent une perte de poids non désirée.
L’efficacité du produit n’a été démontrée qu’avec une administration de 14 jours correspondant aux recommandations actuelles (voir rubrique 4.9). La répétition du traitement n’a pas a été testée et, à ce titre, ne devrait être effectuée qu’après une évaluation du rapport bénéfice/risque par le vétérinaire.
L’efficacité et l’innocuité du médicament vétérinaire n’ont pas été établies chez les chats pesant moins de 2,1 kg ou plus de 7,0 kg.- Précautions particulières pour une utilisation sûre chez les espèces cibles
Le médicament vétérinaire ne doit pas être appliqué sur une peau lésée. Dans le cas d’une maladie hépatique, des taux élevés d’enzymes hépatiques peuvent être observés. Une maladie rénale peut réduire la clairance de la mirtazapine, ce qui peut donner lieu à une exposition accrue au médicament. Dans ces cas particuliers, les paramètres biochimiques hépatiques et rénaux doivent être surveillés régulièrement pendant le traitement.
Les effets de la mirtazapine sur la régulation du glucose n’ont pas été évalués. En cas d’utilisation chez des chats atteints de diabète sucré, la glycémie doit être surveillée régulièrement.
Chez le chat hypovolémique, un traitement de soutien (fluidothérapie) doit être mis en place.
Il convient de veiller à ce que les autres animaux de la maison ne rentrent pas en contact avec le site d’application avant qu’il ne soit sec.
- Précaution particulière à prendre par la personne qui administre le médicament
Le produit peut être absorbé par voie cutanée ou orale et peut provoquer somnolence ou sédation.
Éviter tout contact direct avec le produit. Éviter tout contact avec l’animal traité pendant les 12 premières heures suivant chaque application quotidienne et jusqu’à ce que le site d’application soit sec. Il est donc recommandé de traiter les animaux le soir. Les animaux traités ne doivent pas être autorisés à dormir avec leurs propriétaires, en particulier les enfants et les femmes enceintes pendant toute la durée du traitement.
Des gants de protection imperméables jetables doivent être fournis avec le produit au point de vente et doivent être portés lors de la manipulation et de l’administration du médicament vétérinaire.
Se laver soigneusement les mains immédiatement après l’administration du médicament vétérinaire ou en cas de contact cutané avec le produit ou le chat traité.
Les informations disponibles concernant la toxicité de la mirtazapine pour la reproduction sont limitées. Étant donné que les femmes enceintes sont considérées comme une population plus sensible, il est recommandé aux femmes enceintes ou à celles qui essaient de concevoir d’éviter de manipuler le produit et d’éviter tout contact avec les animaux traités pendant la période de traitement.
Le produit peut être nocif après ingestion.
Ne pas laisser le tube avec sécurité-enfants hors de la boîte, sauf pendant la phase d’application. Après utilisation, le tube avec sécurité-enfants doit être replacé immédiatement dans la boîte. Les enfants ne doivent pas être présents lors de l’application du traitement.
Après application, le tube doit être replacé dans la boîte avec sécurité-enfants ou le flacon avec un bouchon sécurité enfants, qui doit être refermé immédiatement.
Ne pas manger, boire ou fumer pendant la manipulation du médicament vétérinaire.
Le médicament vétérinaire est un sensibilisant cutané. Les personnes présentant une hypersensibilité connue à la mirtazapine ne doivent pas manipuler ce médicament vétérinaire.
Ce médicament vétérinaire peut causer une irritation des yeux et de la peau. Éviter de porter les mains à la bouche et aux yeux jusqu’à ce que les mains aient été bien lavées. En cas de contact avec les yeux, rincer abondamment à l’eau claire. En cas de contact avec la peau, se laver soigneusement à l’eau tiède et au savon. En cas d’irritation de la peau ou des yeux ou en cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice.
- Précautions particulières concernant la protection de l'environnement
Aucune.
- Autres précautions
Aucune.
Interactions et cas particuliers
- Utilisation en cas de gravidité, de lactation ou de ponte
Gestation et lactation : Ne pas utiliser en cas de gestation ou de lactation (voir rubrique 4.3 du RCP).
Fertilité : Ne pas utiliser sur les animaux destinés à la reproduction (voir rubrique 4.3 du RCP).
- Interactions médicamenteuses et autres formes d'interactions
La mirtazapine a été identifiée comme potentiellement toxique pour la reproduction chez le rat et chez le lapin.
L’innocuité du médicament vétérinaire n’a pas été établie en cas de gestation ou de lactation.
Ne pas utiliser chez les chats traités avec de la cyproheptadine, du tramadol ou des inhibiteurs de la monoamine oxydase (IMAO) ou ayant été traités avec un IMAO dans les 14 jours précédant le traitement par le médicament vétérinaire car il peut y avoir une augmentation du risque de syndrome sérotoninergique (voir rubrique 4.3).
La mirtazapine peut augmenter les propriétés sédatives des benzodiazépines et d’autres substances ayant des propriétés sédatives (antihistaminiques H1, opiacés). Les concentrations plasmatiques de mirtazapine peuvent également augmenter en cas d’utilisation concomitante avec du kétoconazole ou de la cimétidine.
Effets indésirables et surdosage
- Effets indésirables
Des réactions au site d’application (érythème, croûte, résidu, desquamation/sécheresse, une peau qui se desquame, tremblement de la tête, dermatite ou irritation, alopécie et prurit) et des modifications de comportement (augmentation des vocalisations, hyperactivité, désorientation ou ataxie, léthargie/faiblesse, recherche d’attention et agressivité) ont été très fréquemment observées dans les études cliniques et d’innocuité.
Des vomissements, une polyurie associée à une diminution de la densité urinaire, une élévation de l’azotémie sanguine et une déshydratation ont été fréquemment observés dans les études cliniques et d’innocuité. Selon la gravité des vomissements, de la déshydratation ou des changements de comportement, l’administration du produit peut être interrompue, en fonction de l’évaluation du rapport bénéfice/risque faite par le vétérinaire.
Ces effets indésirables, y compris les réactions locales, ont disparu à la fin de la période de traitement, sans traitement spécifique.
En de rares occasions, des réactions d’hypersensibilité peuvent survenir. Dans ce cas, le traitement doit être immédiatement interrompu.
En cas d’ingestion par voie orale, en plus des effets mentionnés ci-dessus (exceptées les réactions locales), une salivation et des tremblements peuvent se produire, en de rares occasions.La fréquence des effets indésirables est définie comme suit :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 animaux traités)
- fréquent (entre 1 et 10 animaux sur 100 animaux traités)
- peu fréquent (entre 1 et 10 animaux sur 1 000 animaux traités)
- rare (entre 1 et 10 animaux sur 10 000 animaux traités)
- très rare (moins d’un animal sur 10 000 animaux traités, y compris les cas isolés).
Posologie
| Espèce(s) | Posologie |
|---|---|
|
Usage transdermique. Le médicament vétérinaire est appliqué par voie topique sur le pavillon interne (face interne de l’oreille) une fois par jour pendant 14 jours, à raison de 0,1 g de pommade par chat (2 mg de mirtazapine par chat). Cela correspond à une ligne de pommade de 3,8 cm (voir ci-dessous).
La dose fixe recommandée a été testée chez des chats pesant entre 2,1 kg et 7,0 kg. Pour appliquer le médicament vétérinaire :
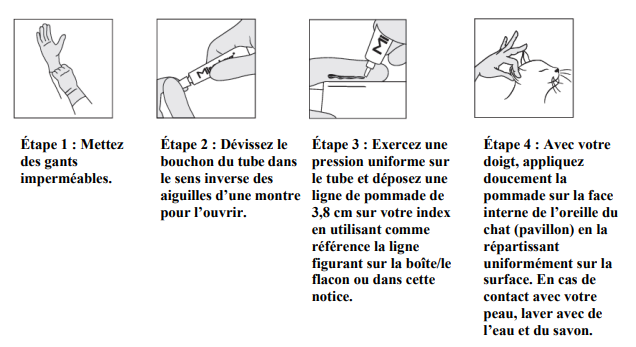 La ligne ci-dessous correspond à la longueur appropriée de la pommade à appliquer : |
Temps d'attente
- Voie d'administration
- Transdermique
Conservation et stockage
- Température de conservation
Pas de précautions particulières de conservation.
Le tube avec sécurité-enfants doit être refermé et replacé immédiatement dans la boîte après chaque utilisation.- Précautions particulières de conservation selon pertinence
Le produit peut être absorbé par voie cutanée ou orale et peut provoquer somnolence ou sédation.
Éviter tout contact direct avec le produit. Éviter tout contact avec l’animal traité pendant les 12 premières heures suivant chaque application quotidienne et jusqu’à ce que le site d’application soit sec. Il est donc recommandé de traiter les animaux le soir. Les animaux traités ne doivent pas être autorisés à dormir avec leurs propriétaires, en particulier les enfants et les femmes enceintes pendant toute la durée du traitement.
Des gants de protection imperméables jetables doivent être fournis avec le produit au point de vente et doivent être portés lors de la manipulation et de l’administration du médicament vétérinaire.
Se laver soigneusement les mains immédiatement après l’administration du médicament vétérinaire ou en cas de contact cutané avec le produit ou le chat traité.
Les informations disponibles concernant la toxicité de la mirtazapine pour la reproduction sont limitées. Étant donné que les femmes enceintes sont considérées comme une population plus sensible, il est recommandé aux femmes enceintes ou à celles qui essaient de concevoir d’éviter de manipuler le produit et d’éviter tout contact avec les animaux traités pendant la période de traitement.
Le produit peut être nocif après ingestion.
Ne pas laisser le tube hors de la boîte avec sécurité-enfants ou le flacon muni d’un bouchon sécurité enfants, sauf pendant la phase d’application. Les enfants ne doivent pas être présents lors de l’application du traitement.
Après application, le tube doit être replacé dans la boîte avec sécurité-enfants ou le flacon avec un bouchon sécurité enfants, qui doit être refermé immédiatement.
Ne pas manger, boire ou fumer pendant la manipulation du médicament vétérinaire.
Le médicament vétérinaire est un sensibilisant cutané. Les personnes présentant une hypersensibilité connue à la mirtazapine ne doivent pas manipuler ce médicament vétérinaire.
Ce médicament vétérinaire peut causer une irritation des yeux et de la peau. Éviter de porter les mains à la bouche et aux yeux jusqu’à ce que les mains aient été bien lavées. En cas de contact avec les yeux, rincer abondamment à l’eau claire. En cas de contact avec la peau, se laver soigneusement à l’eau tiède et au savon. En cas d’irritation de la peau ou des yeux ou en cas d’ingestion accidentelle, demandez immédiatement conseil à un médecin et montrez-lui la notice.- Précaution particulière à prendre lors de l'élimination
Tous médicaments vétérinaires non utilisés ou déchets dérivés de ces médicaments doivent être éliminés conformément aux exigences locales.
Informations commerciales
| Présentation | Accessible au groupement | Classement du médicament en matière de délivrance | Numéro d'autorisation de mise sur le marché |
|---|---|---|---|
| MIRATAZ® 20 mg/g Pommade transdermique pour chats Tube de 3 g | Oui | Soumis à prescription | EU/2/19/247/003 (Tube [PE] avec sécurité-enfants [dans une boîte en carton]) |
Informations de révision
- Date de révision de la notice
- 1/1/1970
Responsabilités
- Titulaire de l'autorisation de mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la mise sur le marché
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUXhttps://www.dechra.fr/
- Responsable de la pharmacovigilance
- DECHRA Veterinary Products SAS
- 60 avenue du Centre
78180 MONTIGNY-LE-BRETONNEUX01.30.48.71.40
https://www.dechra.fr/

