KELACTIN® 50 µg/mL Solution buvable pour chiens et chats
Laboratoire DESTAINGSolution buvable
Composition
Principes actifs et excipients
Principes actifs
| Nom du principe actif | Quantité de principe actif |
|---|---|
| Cabergoline | 50 µg |
Excipients
| Nom de l'excipient |
|---|
| Triglycérides à chaîne moyenne |
| Azote, faible teneur en oxygène |
Clinique
Indications d'utilisation par espèce
- Chienne
Chez la chienne :
- Traitement de la pseudo-gestation.
Tarissement de la sécrétion lactée.
- Chatte
- Chez la chatte :
Tarissement de la sécrétion lactée.
Voie d'administration et posologie
Voie d'administration
- Orale
Posologie
- Chienne
- Chatte
Le médicament vétérinaire doit être administré oralement, soit directement dans la bouche, soit mélangé à la nourriture.
La dose est de 0,1 ml/kg de poids corporel (ce qui équivaut à 5 µg/kg de poids corporel de cabergoline) une fois par jour pendant 4 à 6 jours consécutifs, en fonction de la gravité de l'état clinique.
Si les symptômes ne disparaissent pas après un seul cycle de traitement ou s'ils réapparaissent après la fin du traitement, on peut répéter le cycle de traitement.Le poids des animaux traités doit être déterminé de manière précise avant l'administration.
Comment prélever le volume recommandé dans le flacon ?
Il est recommandé d'utiliser l'adaptateur de flacon et la seringue inclus dans l'emballage pour retirer le médicament vétérinaire du flacon. Pour cela, les étapes suivantes sont nécessaires :Préparation du flacon pour la première utilisation :
Placer le flacon sur une surface plane. Placer l’adaptateur sur le dessus du flacon à la verticale de façon à ce que la pointe de l’adaptateur transperce le bouchon en son centre. Fixer solidement l’adaptateur sur le flacon en l’enfonçant.
Dès lors, l’adaptateur reste fixé en permanence sur le flacon. Cela permet au flacon de rester solidement scellé et de disposer d’un produit prêt à l’emploi jusqu’à ce que le flacon soit vide.
Prélèvement de la quantité requise/prescrite :
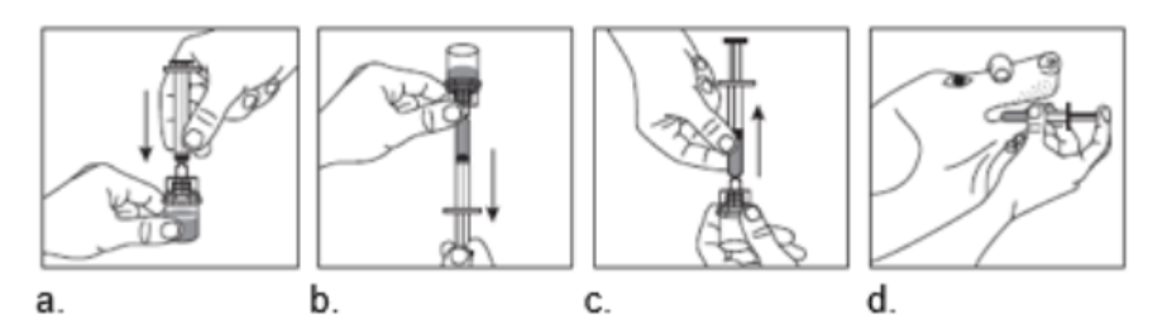
a. Fixer la seringue à l’adaptateur en enfonçant fermement la seringue dans l’adaptateur pour flacon, de manière à éviter toute fuite du médicament vétérinaire lors du prélèvement de la dose du flacon.
b. Retourner et aspirer le médicament vétérinaire au départ du flacon dans la seringue en maintenant le flacon la tête en bas.
c. Retirer la seringue de l’adaptateur en la tenant à la verticale. Laisser l’adaptateur sur le flacon.
d. Le médicament vétérinaire est à présent prêt à être administré.
Il est recommandé de rincer et de sécher la seringue après chaque application. Pour le prochain prélèvement du produit, reprendre à l’étape a.
Temps d'attente
- Chien
- Chienne
- Chat
- Chatte
Denrée Durée Unité Voie(s) d'administration 0 Sans objet
Complément d'information temps d'attente
Sans objet.
Contre indications
- Ne pas utiliser chez les animaux gestants car ce produit peut provoquer un avortement.
Ne pas utiliser en association avec un antagoniste de la dopamine. - Ne pas utiliser en cas d'hypersensibilité à la substance active ou à l'un des excipients.
La cabergoline est susceptible d'induire une hypotension transitoire chez les animaux traités. Ne pas utiliser chez les animaux traités concomitamment par des médicaments hypotenseurs. Ne pas utiliser immédiatement après une intervention chirurgicale, lorsque l'animal est encore sous l'influence de produits anesthésiques.
Mises en garde particulières à chaque espèce cible
Un traitement hygiénique complémentaire doit inclure une restriction de la consommation d'eau et de glucides et une augmentation de l'exercice.
Précautions particulières d'emploi
Précautions particulières pour une utilisation sûre chez les espèces cibles
Sans objet.
Précautions particulières à prendre par la personne qui administre le médicament
Se laver les mains après utilisation. Éviter tout contact avec la peau, la bouche ou les yeux. Nettoyer immédiatement les éventuelles éclaboussures.
Les femmes en âge d'avoir des enfants et les femmes qui allaitent ne doivent pas manipuler le produit ou doivent porter des gants jetables lors de l'administration du produit.
Les personnes présentant une hypersensibilité connue à la cabergoline ou à l'un des autres ingrédients du produit devraient éviter tout contact avec le médicament vétérinaire.
Ne pas laisser de seringues pleines sans surveillance en présence d'enfants. En cas d'ingestion accidentelle, en particulier par un enfant, demander immédiatement conseil à un médecin et montrez-lui la notice ou l'étiquetage
Précautions particulières concernant la protection de l'environnement
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Autres précautions
Aucune.
Interactions médicamenteuses et autres formes d'interaction
Comme la cabergoline agit par stimulation directe des récepteurs de la dopamine, le produit ne doit pas être administré en même temps que des médicaments dotés d'une activité antagoniste de la dopamine (par exemple phénothiazines, butyrophénones, métoclopramide), car ces derniers risquent de diminuer ses effets inhibiteurs de la prolactine.
La cabergoline pouvant induire une hypotension transitoire, le produit ne doit pas être administré à des animaux traités simultanément par des médicaments hypotenseurs.
Utilisation en cas de gravidité de lactation ou de ponte
La cabergoline peut provoquer un avortement à un stade avancé de la gestation et ne doit pas être utilisée chez les animaux gestants. Un diagnostic différentiel entre une gestation et une pseudo-gestation doit être correctement établi.
Le produit est indiqué pour le tarissement de la sécrétion lactée : l'inhibition de la sécrétion de prolactine par la cabergoline induit un arrêt rapide de la lactation et une réduction de la taille des glandes mammaires. Le produit ne doit pas être utilisé chez les animaux qui allaitent, sauf si un tarissement est nécessaire.
Effets indésirables
Les effets indésirables potentiels sont :
- somnolence ;
- anorexie ;
- vomissements.
Ces effets indésirables sont généralement d'intensité modérée et transitoires.
Des vomissements ne surviennent généralement qu'après la première administration. En pareil cas, il n'est pas nécessaire d'interrompre le traitement, car les vomissements ne se reproduiront pas après l'administration suivante.
Dans de très rares cas, des réactions allergiques telles qu'œdème, urticaire, dermatite et prurit sont susceptibles de se produire.
Dans de très rares cas, une hypotension transitoire est susceptible de se produire.
Dans de très rares cas, des symptômes neurologiques tels que somnolence, tremblements musculaires, ataxie, hyperactivité et convulsions sont susceptibles de se produire.
La fréquence des effets indésirables est définie en utilisant la convention suivante :
- très fréquent (effets indésirables chez plus d’1 animal sur 10 au cours d’un traitement)
- fréquent (entre 1 et 10 animaux sur 100)
- peu fréquent (entre 1 et 10 animaux sur 1 000)
- rare (entre 1 et 10 animaux sur 10 000)
- très rare (moins d’un animal sur 10 000, y compris les cas isolés).
Surdosage (symptômes, conduite d’urgences, antidotes)
Les données expérimentales indiquent qu'un surdosage unique de cabergoline est susceptible d'entraîner un risque accru de vomissements après traitement et éventuellement une augmentation de l'hypotension après traitement.
Mettre en place des mesures générales de soutien en vue d'éliminer le médicament non absorbé et de maintenir la tension artérielle si nécessaire. Comme antidote, on peut envisager l'administration parentérale d'antagonistes de la dopamine tels que la métoclopramide.
Informations pharmacologiques ou immunologiques
codes ATC
QG02CB03 : cabergoline
Pharmacodynamie
La pharmacodynamie de la cabergoline a été étudiée dans divers systèmes in vitro et in vivo. Les principales observations peuvent être résumées comme suit :
La cabergoline est un puissant inhibiteur de la sécrétion de prolactine par l'hypophyse et, par conséquent, inhibe les processus qui dépendent de la sécrétion de prolactine tels que la lactation.
Le mécanisme d'action de la cabergoline est une interaction directe avec les récepteurs dopaminergiques D-2 des cellules lactotropes hypophysaires ; cette interaction a un effet persistant.
La cabergoline présente une certaine affinité pour les récepteurs noradrénergiques, mais n'affecte pas le métabolisme de la noradrénaline ou de la sérotonine.
Comme les autres dérivés de l'ergoline, la cabergoline a des effets émétiques (équivalents en puissance à ceux du pergolide et de la bromocriptine).
À fortes doses par voie orale, la cabergoline induit une baisse de la tension artérielle.
Pharmacocinétique et environnement
Il n'y a pas de données pharmacocinétiques disponibles pour le schéma d'administration recommandé chez le chien et le chat.
Des études pharmacocinétiques ont été réalisées chez le chien à une dose journalière de 80 µg/kg de poids corporel (16 fois la dose recommandée). Les chiens ont été traités pendant 30 jours ; des évaluations pharmacocinétiques ont eu lieu au jour 1 et au jour 28.
- Absorption
Tmax = 1 heure au jour 1 et 0,5 à 2 heures (moyenne : 75 minutes) au jour 28 ;
Cmax variant de 1140 à 3155 pg/mL (moyenne : 2147 pg/mL) au jour 1 et de 455 à 4217 pg/mL (moyenne : 2336 pg/mL) au jour 28 ;
AUC(0-24 h) variant de 3896 à 10216 pg.h.mL-1 (moyenne : 7056 pg.h.mL-1) au jour 1 et de 3231 à 19043 pg.h.mL-1 (moyenne : 11137 pg.h.mL-1) au jour 28.
- Élimination
Demi-vie plasmatique chez le chien : t1/2 au jour 1 ~ 19 heures ; t1/2 au jour 28 ~ 10 heures.
Données pharmaceutiques
Incompatibilités majeures
Ne pas mélanger le produit avec une solution aqueuse (par exemple du lait).
En l'absence d'études de compatibilité, ce médicament vétérinaire ne doit pas être mélangé avec d'autres médicaments vétérinaires.
Durée de conservation
Durée de conservation du médicament vétérinaire tel que conditionné pour la vente : 2 ans.
Durée de conservation après ouverture
Durée de conservation après première ouverture du conditionnement primaire : 14 jours.
Température de conservation après ouverture
Après première ouverture : à conserver à une température ne dépassant pas 25°C.
Température de conservation
Tel que conditionné pour la vente : à conserver au réfrigérateur (entre +2°C et +8°C).
Précautions particulières de conservation selon pertinence
Conserver en position verticale.
Conserver le flacon dans la boîte en carton afin de le protéger de la lumière.
Ne pas congeler.
Précautions particulières à prendre lors de l'élimination de médicaments non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Les conditionnements vides et tout reliquat de produit doivent être éliminés suivant les pratiques en vigueur régies par la réglementation sur les déchets.
Nature et composition du conditionnement primaire
Flacon verre coloré de type III (7 mL)
Flacon verre coloré de type III (14 mL)
Flacon verre coloré de type II (24 mL)
Bouchon caoutchouc bromobutyle gris
Capsule aluminium
Titulaire de l'autorisation de mise sur le marché
VEYX-PHARMA
SÖHREWEG 6 34639 SCHWARZENBORN ALLEMAGNE
Présentations commercialisées et AMM
| Présentation | GTIN | Numéro d'autorisation de mise sur le marché | Date de première mise sur le marché (ou AMM) | Classement du médicament en matière de délivrance | Accessible aux groupements |
|---|---|---|---|---|---|
| Boîte contenant 1 flacon de 7 mL, 1 adaptateur et 1 seringue graduée de 1 mL | 05414897037769 | FR/V/2255430 9/2012 | 2/9/2012 | Soumis à prescription | Oui |
| Boîte contenant 1 flacon de 24 mL, 1 adaptateur et 1 seringue graduée de 3 mL | 05414897037783 | FR/V/2255430 9/2012 | 2/9/2012 | Soumis à prescription | Oui |
| Boîte contenant 1 flacon de 14 mL, 1 adaptateur et 1 seringue graduée de 3 mL | 05414897037776 | FR/V/2255430 9/2012 | 2/9/2012 | Soumis à prescription | Oui |
Responsable de la mise sur le marché
Laboratoire DESTAING
45 bd Marcel Pagnol
06130 Grasse
Tél:04.93.42.02.00
Fax:04.93.42.03.00
Responsable de la Pharmacovigilance
Laboratoire DESTAING
45 bd Marcel Pagnol
06130 Grasse
Tél:04.93.42.02.00
Fax:04.93.42.03.00
